

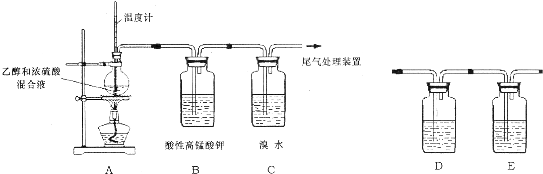
���� ��1�����ݹ�������ͼ��ϵ��յ�ԭ���Լ�����֪ʶ���жϣ�
��2���ٳ�ȥ������ѡ��̼������Һ����ȥþ����ѡ������������Һ����ȥ���������ѡ���Ȼ�����Һ��Ϊ�˱�֤�����ʳ����������Լ����������Ϊ�˲������µ����ʣ�Ӧ���ȼ����������ƣ�Ȼ������Ȼ������ټ���̼���ƣ���������������ÿ���Լ������������֤���������ʶ��ܳ�ȥ����Ӧ����ü��ȷ�������ȥʣ����Ȼ��⣻
�ڸ��ݴ��������ˮ�л����������������Ӷ�װ�õ�Ӱ��Ƕ����ش�
��3�������У��������������������ݵ缫��Ӧȷ��������ݵ��صĹ���ԭ������д����ʽ��
��4���������������ԣ��ܽ�������������Ϊ�����ƣ�
��5����������NaOH���������������ۺĵ�����ʵ�ʺĵ������㣮
��� �⣺��1�����ݹ�������ͼ�����õ���ԭ���Լ��������֪���Ȼ��ơ����������ǿ���ѭ��ʹ�õģ��ʴ�Ϊ���Ȼ��ơ��������ƣ�
����2�����ȼ���������NaOH����ȥþ���ӣ�Ȼ��������BaCl2����ȥSO42-��CO32-���ټ������Na2CO3 ��ȥCa2+������Ba2+�����˺���Һ�м�����������ᣬ��ȥ��Һ��ʣ���̼��������������е��������������ȳ�ȥʣ����Ȼ��⣬Ҳ���ȼ�BaCl2���ټ���NaOH����Ӧ��֤��������μ���Na2CO3��HCl��Ϊ�˽���������ʳ�����̼���Ʊ�������Ȼ����ĺ��棬��D����
�ʴ�Ϊ��D��
�ڴ��������ˮ�л�����������������Mg2+��Ca2+�����������»����ɳ�������װ���еĽ���Ĥ����Ӱ�죬
�ʴ�Ϊ�����Լ����������ˮ�л���������Mg2+��Ca2+�����������»����ɳ����������ӽ���Ĥ��
��3�������У���������������������������B�ǵ�Դ�ĸ�����A��������E���������������ϲ���������������ⱥ��ʳ��ˮ��ԭ������ʽΪ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2OH-���ʴ�Ϊ��H2��������2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2OH-��
��4���������������ԣ��ܽ�������������Ϊ�����ƣ���Na2SO3+Cl2+H2O=Na2SO4+2HCl���ʴ�Ϊ��Na2SO3+Cl2+H2O=Na2SO4+2HCl��
��5���ռ���Һ����Ϊ1.342��103kg/m3��113m3=1.516��105kg��
m��NaOH��=1.516��105kg��32%=4.85��104kg��
����������Ҫ������Ϊ$\frac{4.85��{10}^{7}g}{1.492g}$=3.252��107A��
��ʵ���Ϻĵ���Ϊ1.45��104A��8��300=3.48��107A��
�õ��۵ĵ��Ч��Ϊ$\frac{3.252}{3.48}$��100%=93.45%��
�ʴ�Ϊ��93.45%��
���� �������ȼҵΪ���壬����ѧ������ѧ����������Ľ��ⷽ��֪ʶ��ע����صĹ���ԭ�������Ӧ���ǹؼ����ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������ڱ��У������߸����ڣ����������ڡ��ĸ������� | |
| B�� | Ԫ�����ڱ���7�����壬7�����壬1��0�壬1�����壬��16���� | |
| C�� | ������Ԫ�أ���ָһ�����������ڣ��ֱ���2��8��8��Ԫ�� | |
| D�� | ��A�еĽ���Ԫ�أ���Ϊ�����Ԫ�أ���AԪ���ֳ�Ϊ±��Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��̼��Ƽ��뵽�����У�CO32-+2H+=CO2��+H2O | |
| B�� | ��������ˮ��Ӧ��K+H2O=K++OH-+H2�� | |
| C�� | ��ϡ�����м�������ͭм��Cu+4H++NO3-=Cu2++2H2O+NO�� | |
| D�� | ��ƫ��������Һ��ͨ����CO2��AlO2-+CO2+2H2O=Al��OH��3��+HCO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
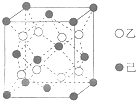 �ҡ������������ӵĺ�������Ų���ͬ��������Ԫ�ذ�6��3��1��ԭ�Ӹ����ȿ��γ�һ�����Ӿ���W����������γɳ������Ӿ���X�����뼺���γɳ������Ӿ���Y����X��Y��������ͬ��
�ҡ������������ӵĺ�������Ų���ͬ��������Ԫ�ذ�6��3��1��ԭ�Ӹ����ȿ��γ�һ�����Ӿ���W����������γɳ������Ӿ���X�����뼺���γɳ������Ӿ���Y����X��Y��������ͬ��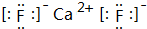 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
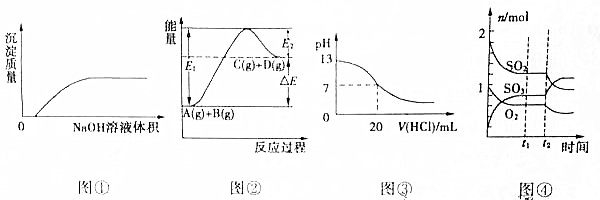
| A�� | ͼ�ٱ�ʾ��NaOH��Һ����Ba��HCO3��2��Һ�� | |
| B�� | ͼ�ڱ�ʾ��Ӧ����ܼ���С����������ܼ��� | |
| C�� | ͼ�۱�ʾ25��ʱ��0.1mol/L�������20mL0.1mol/LNaOH��Һ�У���Һ��pH�����������ı仯���� | |
| D�� | ͼ�ܱ�ʾһ�������µķ�Ӧ2SO2��g��+O2?2SO3��g����H��0��t2ʱ�̸ı�����������ǽ����¶Ȼ���С������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com