
在相同条件下,相同体积的两种烃蒸气,完全燃烧生成的CO2体积比为1∶2,生成水蒸气的体积比为2∶3,则这种烃可能的组合是:
(1)__________________和__________________。
(2)__________________和__________________。
(3)__________________和__________________。
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:阅读理解
| 催化剂 |

| 催化剂 |
| △ |
| 催化剂 |
| △ |
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:




| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |


查看答案和解析>>
科目:高中化学 来源: 题型:





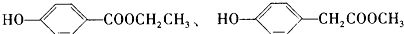 .请写出符合上述条件的其它同分异构体的结构简式
.请写出符合上述条件的其它同分异构体的结构简式

| b |
| 18 |
| 5n |
| 22.4×9 |
| b |
| 18 |
| b |
| 18 |
| 5n |
| 22.4×9 |
| b |
| 18 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
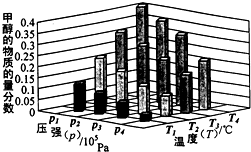 能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.
能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com