
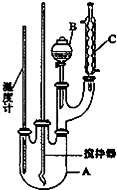
 实验室制备硝基苯的反应原理和实验装置如下:
实验室制备硝基苯的反应原理和实验装置如下: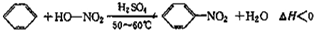
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于水 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
分析 (1)装置C为球形冷凝管,起冷凝回流作用;
(2)配制混酸应防止液体迸溅;
(3)反应在50℃~60℃下进行,利用水浴加热控制;溶有浓硝酸分解产生的NO2等杂质;
(4)用氢氧化钠洗去溶解少量酸,水洗除去未反应的NaOH及生成的盐;
(5)直形冷凝管通常需要通入冷凝水,温差过大容易发生炸裂;
(6)根据苯的质量计算硝基苯的理论产量,产量=(实际产量÷理论产量)×100%.
解答 解:(1)装置C为球形冷凝管,苯与浓硝酸都以挥发,C起冷凝回流作用,提高原料利用率,
故答案为:冷凝回流;
(2)浓硝酸与浓硫酸混合会放出大量的热,如将浓硝酸加入浓硫酸中,硝酸的密度小于浓硫酸,可能为导致液体迸溅,
故答案为:不能,容易发生迸溅;
(3)反应在50℃~60℃下进行,低于水的沸点,可以利用水浴加热控制,受热均匀,便于控制温度,浓硝酸受热易分解,溶有浓硝酸分解产生的NO2(或硝酸)等杂质而呈黄色,
故答案为:水浴加热;溶有浓硝酸分解产生的NO2(或硝酸)等杂质;
(4)先用水洗除去浓硫酸、硝酸,再用氢氧化钠除去溶解的少量酸,最后水洗除去未反应的NaOH及生成的盐,
故答案为:洗去残留的NaOH及生成的盐;
(5)直形冷凝管通常需要通入冷凝水,以免直形冷凝管通水冷却时导致温差过大而发生炸裂,选用空气冷凝管,不选用直形冷凝管,
故答案为:以免直形冷凝管通水冷却时导致温差过大而发生炸裂;
(6)苯完全反应生成硝基苯的理论产量为15.84g×$\frac{123}{78}$,故硝基苯的产率为[18g÷(15.84g×$\frac{123}{78}$)]×100%=72.06%,
故答案为:72.06%.
点评 本题考查有机物制备实验,涉及对装置及操作的分析评价、物质的分离提纯、产率计算等,难度中等,注意操作规范性及仪器作用、渗透安全意识.


科目:高中化学 来源: 题型:选择题
| A. | 用铜电极电解硝酸银溶液:4Ag++2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4H+ | |
| B. | FeS中加入足量稀硝酸:FeS+2 H+=Fe2++H2↑ | |
| C. | 石灰石溶于醋酸溶液中:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| D. | 澄清石灰水中通入过量的CO2:CO2+OH-=HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
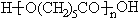 }及阻燃剂四溴双酚A.合成线路如图:
}及阻燃剂四溴双酚A.合成线路如图: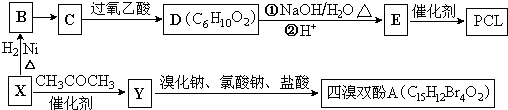
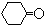
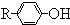 $\stackrel{溴化钠、氯化钠、盐酸}{→}$
$\stackrel{溴化钠、氯化钠、盐酸}{→}$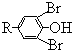
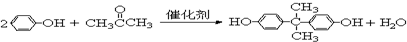 .
.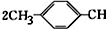 =CH2+2ROH+2CO+O2$\stackrel{一定条件}{→}$
=CH2+2ROH+2CO+O2$\stackrel{一定条件}{→}$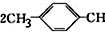 =CHCOOR+2H2O,利用乙烯为有机原料(无机物和反应条件自选)合成聚合物涂料
=CHCOOR+2H2O,利用乙烯为有机原料(无机物和反应条件自选)合成聚合物涂料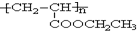 ,写出合成该涂料的反应流程图:
,写出合成该涂料的反应流程图: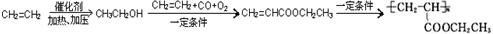 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作和现象 | 结论 | |
| A | 向用盐酸酸化的FeCl2溶液的试管中加入少量NaNO2溶液,在管口观察到红棕色气体 | 主要原因是:H++NO2-═HNO2, 2HNO2═NO↑+NO2↑+H2O |
| B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成. | 淀粉没有水解成葡萄糖 |
| C | 向阿司匹林(乙酰水杨酸)中加足量饱和NaHCO3溶液,有大量气泡产生. | 阿司匹林彻底水解 |
| D | 向1mL1.0mol•L-1AlCl3溶液中滴加2mL10% NH4F溶液,再滴加1mL 3.0mol•L-1NH3•H2O溶液,无沉淀生成. | Al3+更易与F-结合成AlF63- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 ; NH3的VSEPR模型为正四面体;请解释加入乙醇后析出晶体的原因乙醇分子的极性比水弱,由于减小溶剂的极性,降低离子化合物Cu(NH3)4SO4•H2O的溶解度.
; NH3的VSEPR模型为正四面体;请解释加入乙醇后析出晶体的原因乙醇分子的极性比水弱,由于减小溶剂的极性,降低离子化合物Cu(NH3)4SO4•H2O的溶解度. .乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是乙二胺分子间存在氢键而三甲胺没有,由于氢键的作用力比范德华力大,故乙二胺沸点比三甲胺高.
.乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是乙二胺分子间存在氢键而三甲胺没有,由于氢键的作用力比范德华力大,故乙二胺沸点比三甲胺高.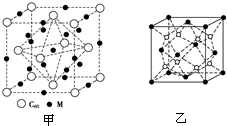
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生活中的玻璃、陶瓷、水泥属于无机硅酸盐材料,其生产原料都需要使用石灰石 | |
| B. | 居室装修材料如化纤地毯、三合板、花岗岩等均会释放出污染空气的甲醛气体 | |
| C. | 侯氏制碱、肥皂的制取工艺过程中均应用了物质溶解度的差异 | |
| D. | 某雨水样品放置一段时间后pH由4.68变为4.28,是因为吸收了CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
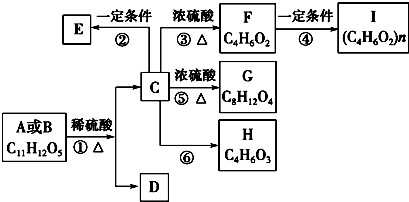
 .
.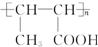
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
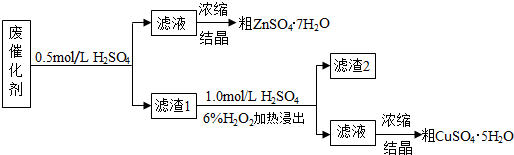

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
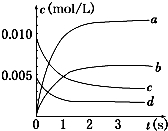 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com