
³£ĪĀĻĀ£¬ŅŃÖŖ0.1mol”¤L-1µÄCH3COOHŗĶHCNČÜŅŗµÄPH·Ö±šĪŖa”¢b£¬ĒŅ1<a< b”£ĻĀĮŠÓŠ¹ŲŠšŹö²»ÕżČ·µÄŹĒ£Ø £©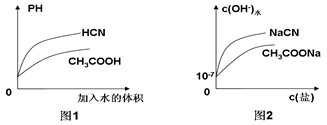
| A£®³£ĪĀĻĀ£¬µČÅØ¶ČµÄCH3COONaČÜŅŗŗĶNaCNČÜŅŗµÄPHĒ°Õß½ĻŠ” |
| B£®ŌŚNaCNČÜŅŗÖŠ£ŗc (Na+£©+ c (H+) £½c (OH-£©+ c (CN-) |
| C£®ĻąĶ¬ĪĀ¶ČĻĀ£¬ĻąĶ¬PHµÄCH3COOHŗĶHCNČÜŅŗ·Ö±š¼ÓĖ®Ļ”ŹĶ£¬ČÜŅŗPHĖęČÜŅŗĢå»ż±ä»ÆµÄĒśĻßČēĶ¼1ĖłŹ¾ |
| D£®³£ĪĀĻĀ£¬CH3COONaČÜŅŗŗĶNaCNČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc(OH-)ÓėŃĪÅØ¶ČµÄ±ä»ÆĒśĻßČēĶ¼2ĖłŹ¾ |
C
½āĪöŹŌĢā·ÖĪö£ŗŌŚĻąĶ¬µÄĶā½ēĢõ¼žĻĀ£¬ĻąĶ¬CH3COOHŗĶHCNČÜŅŗµÄPHĒ°Õߊ”ÓŚŗóÕߣ¬ŌņCH3COOHµÄĖįŠŌ“óÓŚHCN ”£A£®CH3COONa”¢NaCN¶¼ŹĒĒæ¼īČõĖįŃĪ£¬Ė®½āŹ¹ČÜŅŗ¼īŠŌ”£ĖįŌ½Čõ£¬ŃĪµÄĖ®½ā³Ģ¶Č¾ĶŌ½“󣬵±ŃĪµÄÅضČĻąµČŹ±£¬ČÜŅŗµÄpH¾ĶŌ½Š”£¬Ņņ“Ė³£ĪĀĻĀ£¬µČÅØ¶ČµÄCH3COONaČÜŅŗŗĶNaCNČÜŅŗµÄPHĒ°Õß½ĻŠ”£¬ÕżČ·£»B£®ŌŚNaCNČÜŅŗÖŠ£¬øł¾ŻµēŗÉŹŲŗćæÉµĆ£ŗc (Na+£©+ c (H+) £½c (OH-£©+ c (CN-)£¬ÕżČ·£»C£®ĻąĶ¬ĪĀ¶ČĻĀ£¬ĻąĶ¬PHµÄCH3COOHŗĶHCNČÜŅŗĒ°ÕßµÄÅØ¶ČŠ”ÓŚŗóÕߣ¬ĖłŅŌ·Ö±š¼ÓĖ®Ļ”ŹĶ£¬ŗóÕߵĵēĄėĘ½ŗāŅĘ¶ÆŹ¹ČÜŅŗÖŠH+ÅضČŌö“óµÄĒ÷ŹĘ“óÓŚĒ°Õߣ¬Ņņ“ĖČÜŅŗPHĖęČÜŅŗĢå»ż±ä»ÆµÄĒśĻßÖŠ“×ĖįµÄŌŚÉĻ±ß£¬HCNµÄŌŚĻĀ±ß£¬“ķĪó£»D£®ÓÉÓŚĖįŠŌCH3COOH>HCN,ĖłŅŌ³£ĪĀĻĀ£¬CH3COONaČÜŅŗŗĶNaCNČÜŅŗÖŠŗóÕßĖ®½ā³Ģ¶Č“ó”£Ņņ“ĖÓÉĖ®µēĄė³öµÄc(OH-)ŗóÕß“óÓŚĒ°Õߣ¬ŃĪµÄÅضČŌ½“ó£¬ŃĪĖ®½ā²śÉśµÄc(OH-)¾ĶŌ½“󔣹ŹÓėŃĪÅØ¶ČµÄ±ä»ÆĒśĻßČēĶ¼2ĖłŹ¾£¬ÕżČ·”£
æ¼µć£ŗæ¼²éČõĖįµÄµēĄė¼°ĘäŃĪČÜŅŗĖ®½āµÄĖį¼īŠŌµÄÖŖŹ¶”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
Įņ“śĮņĖįÄĘ(Na2S2O3)Ė×³Ę“óĖÕ“ņ£¬ÕÕĻąŅµÖŠÓĆ×÷¶ØÓ°¼Į”£Na2S2O3Ņ×ČÜÓŚĖ®£¬ŌŚĖįŠŌČÜŅŗÖŠÓėĖį·“Ó¦ÓŠµ„ÖŹĮņŗĶSO2Éś³É”£
£Ø1£©Na2S2O3ČÜŅŗÓėĻ”ĮņĖį»ģŗĻ·“Ó¦æÉÓĆÓŚĢ½¾æĶā½ēĢõ¼ž¶Ō·“Ó¦ĖŁĀŹµÄÓ°Ļģ£¬Ķź³ÉÓŠ¹ŲµÄŹµŃéÉč¼Ę±ķ(ŅŃÖŖø÷ČÜŅŗĢå»ż¾łĪŖ5 mL)£ŗ
| ŹµŃ鱹ŗÅ | T/K | c(Na2S2O3)/ mol”¤L£1 | c(H2SO4)/ mol”¤L£1 | ŹµŃéÄæµÄ |
| ¢Ł | 298 | 0.1 | 0.1 | ŹµŃé¢ŁŗĶ¢ŚĢ½¾æĪĀ¶Č¶ŌøĆ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£»ŹµŃé¢Ł”¢¢ŪŗĶ¢ÜĢ½¾æ·“Ó¦ĪļÅØ¶Č¶ŌøĆ·“Ó¦ĖŁĀŹµÄÓ°Ļģ |
| ¢Ś | 308 | | | |
| ¢Ū | | 0.2 | | |
| ¢Ü | | 0.1 | |
| ŹµŃé²½Öč | Ō¤ĘŚĻÖĻóŗĶ½įĀŪ |
| ²½Öč1£ŗȔɣĮæ¹ĢĢåÓŚŹŌ¹ÜÖŠ£¬¼ÓÕōĮóĖ®Čܽā | |
| ²½Öč2£ŗ | |
| ²½Öč3£ŗ | |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
°Ń0.05molNaOH¹ĢĢå·Ö±š¼ÓČėĻĀĮŠ100mLČÜŅŗÖŠ£¬ČÜŅŗµÄµ¼µēÄÜĮ¦±ä»Æ²»“óµÄŹĒ£Ø £©
| A£®×ŌĄ“Ė® | B£®0.5mol”¤L”Ŗ1KOHČÜŅŗ |
| C£®0.5mol”¤L”Ŗ1“×Ėį | D£®0.5mol”¤L”Ŗ1NH4ClČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®Ä³ĪĀ¶ČŹ±£¬ 1LpH=6µÄĖ®ČÜŅŗ£¬ŗ¬ Ąė×Ó Ąė×Ó |
B£®ŗ¬10£®6gNa2CO3ČÜŅŗÖŠ£¬Ėłŗ¬ŅõĄė×Ó×ÜŹżµČÓŚ |
| C£®VLamol/LFeCl3ČÜŅŗÖŠ£¬ČōFe3+Ąė×ÓŹżÄæĪŖ1mol£¬ŌņCl-Ąė×ÓŹżÄæ“óÓŚ3mol”£ |
D£®µē½ā¾«Į¶“ÖĶŹ±£¬Ćæ×ŖŅĘ µē×Ó£¬Ńō¼«ÉĻČܽāµÄ µē×Ó£¬Ńō¼«ÉĻČܽāµÄ Ō×ÓŹż±ŲĪŖ Ō×ÓŹż±ŲĪŖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
³£ĪĀĻĀ£¬°ŃpH£½3µÄH2SO4ČÜŅŗŗĶpH£½10µÄNaOHČÜŅŗ»ģŗĻ£¬Į½ÕßĒ”ŗĆÖŠŗĶ£¬ŌņĖįŗĶ¼īµÄĢå»ż±ČÓ¦ŹĒ
| A£®10”Ć1 | B£®1”Ć10 | C£®1”Ć100 | D£®1”Ć2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
¼ŗÖŖ25”ꏱ£¬Ksp(AgCl) =1.8”Į10£10£¬Ksp(AgBr) =5.4”Į10£13£¬Ksp(AgI) =8.5”Į10£17”£Ä³ČÜŅŗÖŠŗ¬ÓŠC1£”¢Br£ŗĶI££¬ÅØ¶Č¾łĪŖ0.010mo1”¤L-1£¬ĻņøĆČÜŅŗÖŠÖšµĪ¼ÓČė0.010mol”¤L£1µÄAgNO3ČÜŅŗŹ±£¬ČżÖÖŅõĄė×Ó²śÉś³ĮµķµÄĻČŗóĖ³ŠņĪŖ
| A£®C1£”¢Br£”¢I£ | B£®Br£”¢C1£”¢I£ |
| C£®I£”¢Br£”¢C1£ | D£®Br£”¢I£”¢C1£ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŅŃÖŖ£ŗCaC2O4³ĮµķµÄKsp=2.3”Į10-9£¬½«µČĢå»żµÄCaCl2ČÜŅŗÓėNa2C2O4ČÜŅŗ»ģŗĻ£¬ČōĘšŹ¼CaCl2µÄÅضČĪŖ1”Į10-2mo1”¤L-1£¬ŌņÉś³É³ĮµķĖłŠčNa2C2O4ČÜŅŗµÄ×īŠ”ĘšŹ¼ÅضČĪŖ
| A£®2. 3”Į10-7mol”¤L-1 | B£®4. 6”Į10-7mol”¤L-1 |
| C£®9. 2”Į10-7mol”¤L-1 | D£® ”Į10-3mol”¤L-1 ”Į10-3mol”¤L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŹŅĪĀĻĀ£¬½«Ņ»ŌŖĖįHAµÄČÜŅŗŗĶKOHČÜŅŗµČĢå»ż»ģŗĻ(ŗöĀŌĢå»ż±ä»Æ)£¬ŹµŃ鏿¾ŻČēĻĀ±ķ£ŗ
| ŹµŃ鱹ŗÅ | ĘšŹ¼ÅضČ/(mol”¤L£1) | ·“Ó¦ŗóČÜŅŗµÄpH | |
| c(HA) | c(KOH) | ||
| ¢Ł | 0.1 | 0.1 | 9 |
| ¢Ś | x | 0.2 | 7 |
 mol/L
mol/L²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”¹ŲĻµ“ķĪóµÄŹĒ
A£®0.1 mol/LµÄNH4ClČÜŅŗÖŠ£ŗ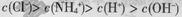 |
B£®0.1mol/LµÄCH3COONaČÜŅŗÖŠ£ŗ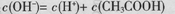 |
C£®0.1 mol/LNa2SµÄČÜŅŗÖŠ£ŗ |
D£®pH=2µÄŃĪĖįÓėpH=12µÄ°±Ė®µČĢå»ż»ģŗĻŗó£ŗ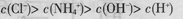 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com