
【题目】(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是 ______。
A.C(s)+H2O(g)═CO(g)+H2(g)△H>0
B.NaOH(aq)+HC1(aq)═NaC1(aq)+H2O(1)△H<0
C.2H2(g)+O2(g)═2H2O(1)△H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极的电极反应式为 ______。
(3)电解原理在化学工业中有着广泛的应用.现将你设计的原电池通过导线与图中电解池相连,其中a为电解液,X和Y均为惰性电极,则:
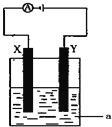
①若a为CuSO4溶液,则电解时的化学反应方程式为 ______ .通电一段时间后,向所得溶液中加入0.2molCuO粉末,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为 ______。
【答案】 C H2+2OH--2e-=2H2O 2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4 0.4mol
2Cu+O2↑+2H2SO4 0.4mol
【解析】(1)能设计成原电池的反应通常是放热反应,同时也必须是氧化还原反应。氢气和氧气反应生成水的反应是一个放热的氧化还原反应,所以在理论上可以设计成原电池,选C。
(2)以KOH溶液为电解质溶液,可以设计一个氢氧燃料电池,其负极上氢气发生氧化反应,电极反应式为 H2+2OH--2e-=2H2O 。
(3)①若a为CuSO4溶液,则电解时,阳极上发生2 H2O-4e-=O2↑+4H+,阴极上发生Cu2++2 e-=Cu,总反应的化学反应方程式为2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4.由电极反应式可知,n(e-)=n(H+),通电一段时间后,向所得溶液中加入0.2molCuO粉末,恰好恢复电解前的浓度和pH。因为0.2molCuO可以与0.4mol H+反应,所以电解过程中转移的电子的物质的量为0.4mol 。
2Cu+O2↑+2H2SO4.由电极反应式可知,n(e-)=n(H+),通电一段时间后,向所得溶液中加入0.2molCuO粉末,恰好恢复电解前的浓度和pH。因为0.2molCuO可以与0.4mol H+反应,所以电解过程中转移的电子的物质的量为0.4mol 。


科目:高中化学 来源: 题型:
【题目】MnO2用途很广,它是一种广泛应用的氧化剂。例如将它加入熔态的玻璃中,可以除去带色的杂质(硫化物或亚铁盐),称为普通玻璃的“漂白剂”。在锰-锌干电池中用作去极剂,以氧化在电极上产生的氢。
(1)Zn- MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。其电解质溶液呈________性(填“酸”、“碱”或“中”),原因是_________________、________________(用离子方程式表示);该电池工作时,电子流向__________极(填“正”或 “负”)。
(2)工业上,常以菱锰矿(主要成分MnCO3,常含有少量铁、钙、锌等元素)为原料,用电解法可以制备MnO2。其制备过程如下:

写出酸浸的主要化学方程式:______________________。
②下图可以看出,从MnSO4和ZnSO4混合溶液中结晶MnSO4·H2O晶体,需要控制的温度范围为______________(填字母)。
A.0~40℃ B.40~60℃ C.60℃以上

③请写出用惰性电极电解MnSO4溶液制备MnO2的阳极反应:___________________。
④该工艺产生的废水中含有较多的Mn2+,通常用H2S或者Na2S溶液处理。25 ℃,在0.10 mol·L-1 H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图(忽略溶液体积的变化、H2S的挥发)。

i.pH=13时,溶液中的c(H2S)+c(HS-)=__________mol·L-1;
ii.某溶液含x mol·L-1 Mn2+、0.10 mol·L-1 H2S,当调节溶液pH=5时,Mn2+开始沉淀,则x= 。[已知:Ksp(MnS)=2.8×10-13]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是几种弱酸常温下的电离平衡常数:
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
则下列说法中不正确的是( )
A. 碳酸的酸性强于氢硫酸
B. 多元弱酸的酸性主要由第一步电离决定
C. 常温下,加水稀释醋酸,![]() 增大
增大
D. 向弱酸溶液中加少量NaOH溶液,电离常数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,在碱性溶液中能大量共存,且溶液为无色透明的是( )
A. K+、MnO4-、Cl-、SO42-
B. Na+、CO32-、SO42-、Cl-
C. NO3-、Na+、HCO3-、Ba2+
D. Na+、NO3-、H+、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列化学仪器:①托盘天平②玻璃棒③药匙④烧杯⑤量筒⑥500mL容量瓶⑦胶头滴管⑧细口试剂瓶⑨标签纸
(1)现有质量分数为98%、密度为1.84gcm﹣3 的浓硫酸,该浓硫酸的浓度为mol/L.若需要配制500mL 1molL硫酸溶液,需用98%的浓硫酸mL.
(2)定容时加蒸馏水至距刻线处改用加水使溶液的凹液面正好与刻线相平.
(3)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响(填写“偏高”“偏低”或“无影响”) ①用以稀释硫酸的烧杯未洗涤
②未经冷却趁热将溶液注入容量瓶
③容量瓶中原有少量的蒸馏水
④定容时观察液面俯视 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯酰胺(H2C=CH—CONH2)具有致癌性和遗传毒性。丙烯酰胺主要是由高碳水化合物、低蛋白质的植物性食物在加热(120 ℃以上)过程中形成,特别在烘烤、油炸时更易形成。丙烯酰胺可以进一步形成在工业上有用的聚丙烯酰胺类物质。
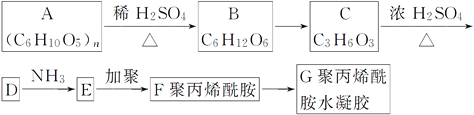
回答下列问题:
(1)D的结构简式为______________;F的结构简式为______________。
(2)指明下列反应类型:A→B____________________,C→D______________________。
(3)丙烯酰胺有多种同分异构体,写出分子中同时含有醛基和碳碳双键的同分异构体:______________________。
(4)写出化学方程式D→E:__________________________________________。2分子C在浓硫酸作用下可形成一个六元酯环,该反应的化学方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用H2还原SiHCl3(沸点:31.85℃)制备纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法正确的是( )

A. 装置Ⅱ、Ⅲ中依次盛装的是浓H2SO4、冰水
B. 实验时,应先加热管式炉,再打开盛装稀硫酸的分液漏斗
C. 为鉴定制得的硅中是否含微量铁单质,需要用到的试剂为盐酸、双氧水、硫氰化钾溶液
D. 该实验中制备氢气的装置也可用于氧氧化钠稀溶液与氯化铵固体反应制备氨气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com