
| A、Cl2既是氧化剂也是还原剂 |
| B、该反应中的电子转移数目为6e- |
| C、氧化剂和还原剂的质量比是1:5 |
| D、NaCl是氧化产物,NaClO3是还原产物 |


科目:高中化学 来源: 题型:
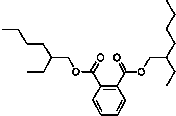 受台湾“塑化剂污染食品”风波的影响,2011年6月1日卫生部紧急发布公告,将塑化剂列入食品中可能违法添加的非食用物质和易滥用的食品添加剂名单.已知塑化剂DEHP分子结构简式如图.下列说法中不正确的是( )
受台湾“塑化剂污染食品”风波的影响,2011年6月1日卫生部紧急发布公告,将塑化剂列入食品中可能违法添加的非食用物质和易滥用的食品添加剂名单.已知塑化剂DEHP分子结构简式如图.下列说法中不正确的是( )| A、DEHP是芳香族化合物 |
| B、DEHP是酯类物质 |
| C、DEHP分子中共有5个双键 |
| D、DEHP分子中至少有8个碳原子在同一平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 压强p(Pa) | 2×105 | 5×105 | 1×106 |
| c(A)mol/L | 0.08 | 0.20 | 0.44 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升高温度,正向反应速率增加,逆向反应速率减小 |
| B、升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
| C、达到平衡后,升高温度有利于该反应平衡正向移动 |
| D、达到平衡后,减小压强有利于该反应平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3(m-n) | ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 溶度积 | 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
| A、五种物质在常温下溶解度最大的是Ag2SO4 |
| B、将氯化银溶解于水后,向其中加入Na2S,则可以生成黑色沉淀 |
| C、AgCl、AgBr和AgI三种物质在常温下的溶解度随着氯、溴、碘的顺序增大 |
| D、沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、高纯度的单质硅被广泛用于制作计算机芯片、制造太阳能电池 |
| B、硅可由二氧化硅还原制得 |
| C、常温时硅与水、空气和酸不反应,但能与氢氟酸反应 |
| D、自然界硅元素的贮量丰富,并存在大量的单质硅 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com