
硼酸(H3BO3)分子的中心原子B最外层电子并未达到饱和,它在水中结合水分子电离出来的OH-使B原子最外层电子达到饱和,电离过程如下图所示。下列表述正确的是( )
A.硼酸加入水中抑制水的电离 B.硼酸是三元酸
C.硼酸与强碱在溶液中反应:H3BO3+OH-→[B(OH)4]- D.硼酸是两性化合物
科目:高中化学 来源: 题型:
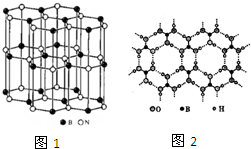 尿素(
尿素(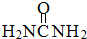 )和硼砂(Na2B4O7)在高温高压下反应可以获得硼氮化合物:
)和硼砂(Na2B4O7)在高温高压下反应可以获得硼氮化合物:查看答案和解析>>
科目:高中化学 来源:2011-2012年重庆西南大学附中高二下学期期中考试化学试卷(带解析) 题型:填空题
(14分)硼酸(H3BO3)是一种片层状结构的白色晶体(下图),有滑腻感,可做润滑剂。硼酸对人体受伤组织有缓和和防腐作用,故可以用于医药和食品防腐等方面。回答下列问题:
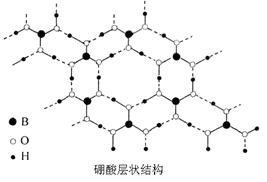
(1)B原子结构示意图为_______________________。
(2)硼酸为一元弱酸,在水中电离方程式为H3BO3+H2O [B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式_______________________________________________。
[B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式_______________________________________________。
(3)下列有关硼酸晶体的说法正确的是_______________。
A、H3BO3分子的稳定性与氢键有关
B、平均1 mol H3BO3的晶体中有3 mol氢键
C、硼酸晶体中层与层之间作用力是范德华力
D、B为sp2杂化,同一层内主要作用力是共价键和氢键
(4)根据对角线规则,与B性质相似的元素是________。
(5)含氧酸的通式为(HO)mROn,根据非羟基氧原子数判断,与H3BO3酸性最接近的是______。
A HClO B.H4SiO4 C.H3PO4 D.HNO2
(6)一种硼酸盐的阴离子为B3O6n-,n=______;B3O6n-结构中只有一个六元环,B的空间化学环境相同,O有两种空间化学环境,画出B3O6n-的结构图(注明所带电荷数):
____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省通许县丽星中学高二下学期期末考试化学试卷(带解析) 题型:填空题
(10分)配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一提供空轨道的粒子结合。如NH4+就是由NH3(氮原子提供电子对)和H+(提供空轨道)通过配位键形成的。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是________。
| A.CO2 | B.H3O+ | C.CH4 | D.NH4+ |
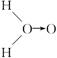 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)查看答案和解析>>
科目:高中化学 来源:2013届河南省高二下学期期末考试化学试卷(解析版) 题型:填空题
(10分)配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一提供空轨道的粒子结合。如NH4+就是由NH3(氮原子提供电子对)和H+(提供空轨道)通过配位键形成的。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是________。
A.CO2 B.H3O+ C.CH4 D.NH4+
(2)硼酸(H3BO3)溶液呈酸性,试写出其电离方程式: _____________________________。
(3)科学家对H2O2结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:
甲: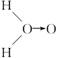 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
乙:HOOH
化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂)。
①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式)________________。
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(共12分)
(1) cis-Pt(NH3)2Cl2、cis-Pt(NH3)2Cl4和cis-PtCl2(en)等是目前临床上广泛使用的抗癌药物,尤其对早期的睾丸癌具有很高的治愈率。实验测得它们都是反磁性物质。(en为乙二胺)
① Pt2+和Pt4+的价电子构型分别为 和 ,上述配合物都是 型(填“内轨”或“外轨”)配合物,cis-Pt(NH3)2Cl2的中心离子杂化轨道类型为 。
② 以上3种抗癌药均为顺式(cis-)结构,而所有的反式(trans-)异构体均无抗癌效果。试画出上述3种物质顺式异构体的结构图:
(2) 已知反应CO(g)+2H2(g)![]() CH3OH(g)在773K时的
CH3OH(g)在773K时的![]() =4.78×10-6。若向某容器中加入1molCO和2 mol H2,在773K达到平衡时,生成0.1mol CH3OH,此时反应体系的压强为 。
=4.78×10-6。若向某容器中加入1molCO和2 mol H2,在773K达到平衡时,生成0.1mol CH3OH,此时反应体系的压强为 。
(3) 称取含硼砂及硼酸的试样0.7513g,用0.1000mol/L HCl标准溶液滴定,以甲基红为指示剂,消耗盐酸25.00mL,再加甘露醇强化后,以酚酞为指示剂,用0.2000mol/L NaOH标准溶液滴定消耗37.50mL。则可知试样中Na2B4O7?10H2O的质量分数为 ,H3BO3的质量分数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com