
£Ø10·Ö£©
¢ń ÅضČĪŖ0.1 mol”¤L£1µÄŃĪĖį”¢ĮņĖį”¢“×ĖįČżÖÖČÜŅŗ£¬ŹŌ»Ų“š£ŗ
(1)ČżÖÖČÜŅŗÖŠc(H£«)ŅĄ“ĪĪŖa mol”¤L£1£¬b mol”¤L£1£¬c mol”¤L£1£¬ĘäÓɓ󵽊”µÄĖ³ŠņŹĒ________”£
(2)ĶźČ«ÖŠŗĶŅ»¶ØĮæNaOHČÜŅŗŹ±£¬ŠčÉĻŹöČżÖÖĖįµÄĢå»żŅĄ“ĪŹĒV1L”¢V2L”¢V3L£¬Ęä“󊔹ŲĻµĪŖ__________________________________”£
(3)ÓėŠæ·“Ó¦æŖŹ¼Ź±²śÉśĒāĘųµÄĖŁĀŹ·Ö±šĪŖv1”¢v2”¢v3£¬ĘäÓɓ󵽊”µÄĖ³ŠņŹĒ________”£
¢ņ c(H+)ĻąĶ¬µÄŃĪĖį”¢ĮņĖį”¢“×ĖįČżÖÖČÜŅŗ£¬ŹŌ»Ų“š£ŗ
(1)ČżÖÖČÜŅŗ¾ł¼ÓĖ®Ļ”ŹĶÖĮĢå»żĪŖŌĄ“µÄ10±¶, c(H+)ŅĄ“ĪĪŖa mol”¤L£1£¬b mol”¤L£1£¬c mol”¤L£1£¬ĘäÓɓ󵽊”µÄĖ³ŠņŹĒ_______”£
(2)ČżÖÖČÜŅŗĢå»żĻąĶ¬Ź±,Ķ¬Ź±¼ÓČėĻąĶ¬µÄŠæ,Čō²śÉśĻąĶ¬ĪļÖŹµÄĮæµÄĒāĘų£¬ĖłŠčŹ±¼ä·Ö±šĪŖt1”¢t2”¢t3£¬Ęä“󊔹ŲĻµŹĒ___________.
¢ń¢Åbac ¢ĘV1=2V2=V3 ¢Ēbac ¢ņ¢Åc£¾a="b" ¢Ęt1=t2£¾t3
½āĪöŹŌĢā·ÖĪö£ŗ¢ń.
£Ø1£©ŃĪĖįc(H£«)=0.1mol/L”¢ĮņĖįc(H£«)=0.2mol/L”¢“×Ėįc(H£«)£¼0.1mol/L£¬¹Źb£¾a£¾c”£
£Ø2£©ÅضČĻąĶ¬µÄ“×Ėį£¬ŃĪĖį£¬ĮņĖį£¬ČżÕßµÄČÜŅŗÖŠH+ÅØ¶Č¹ŲĻµĪŖĮņĖį£¾ŃĪĖį£¾“×Ėį£¬ŅņĪŖĮņĖįĪŖ¶žŌŖĖį£¬H+ÅضČĪŖŃĪĖįµēĄė³öH+ÅØ¶ČµÄ2±¶£¬¶ų“×ĖįĪŖČõĖį£¬²æ·ÖµēĄėĖłŅŌH+ÅØ¶ČŹĒ×īŠ”µÄ£¬µ«×ܵÄH+µÄÅØ¶Č¹ŲĻµĪŖŃĪĖį=“×Ėį£¼ĮņĖį£¬ŃĪĖįŗĶĮņĖįĪŖĒæĖįĶźČ«µēĄė£¬ĖłŅŌÖŠŗĶNaOHĖłŠčµÄĖįµÄĢå»ż¹ŲĻµĪŖ“×Ėį=ŃĪĖį£¾ĮņĖį£¬¼“V1=2V2=V3”£
£Ø3£©ÓėŠæ·“Ó¦£¬·“Ó¦ĖŁĀŹÓėČÜŅŗÖŠµÄH+µÄÅضČÓŠ¹Ų£¬H+µÄÅØ¶Č¹ŲĻµĪŖĮņĖį£¾ŃĪĖį£¾“×Ėį£¬ĖłŅŌ³õŹ¼·“Ó¦ĖŁĀŹ¹ŲĻµĪŖĮņĖį£¾ŃĪĖį£¾“×Ėį£¬¼“v2£¾v1£¾v3”£
¢ņ.
£Ø1£©ČżÖÖČÜŅŗ¾ł¼ÓĖ®Ļ”ŹĶÖĮĢå»żĪŖŌĄ“µÄ10±¶, ŃĪĖį”¢ĮņĖįŹĒĒæµē½āÖŹĶźČ«µēĄė£¬ĖłŅŌc(H£«)¶¼¼õŠ”ĪŖŌĄ“µÄ1/10£¬“×ĖįŹĒČõµē½āÖŹ£¬¼ÓĖ®Ļ”ŹĶ»įÓŠ²æ·ÖĒāĄė×ÓÓÖµēĄė“¦Ąķ£¬ĖłŅŌc(H£«)²»»į¼õŠ”µ½ŌĄ“µÄ1/10”£¹Źc(H£«) Óɓ󵽊”µÄĖ³ŠņŹĒc£¾a=b”£
£Ø2£©ČżÖÖČÜŅŗĢå»żĻąĶ¬Ź±,Ķ¬Ź±¼ÓČėĻąĶ¬µÄŠæ,Čō²śÉśĻąĶ¬ĪļÖŹµÄĮæµÄĒāĘų£¬ĖłŠčŹ±¼äÓÉÓŚŃĪĖį”¢ĮņĖįc(H£«)ĻąµČ”£ĖłŅŌt1=t2”£“×ĖįŹĒČõµē½āÖŹ£¬Ö»ÓŠ²æ·ÖĒāĄė×ÓµēĄė³öĄ“”£Ėę×Å·“Ó¦µÄ½ųŠŠ£¬»į¼ĢŠųµēĄė³öĒāĄė×Ó”£ĖłŅŌ“×Ėįc(H£«)»į±ČŃĪĖį”¢ĮņĖįc(H£«)“󔣹Ź“×Ėį·“Ó¦ĖłŠčŹ±¼ä×ī¶Ģ”£t1=t2£¾t3”£
æ¼µć£ŗµē½āÖŹµÄµēĄė
µćĘĄ£ŗ±¾Ģā×¢Ņā°ŃĪÕ“×ĖįµÄ²æ·ÖµēĄė¶Ōc(H£«)µÄÓ°Ļģ”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
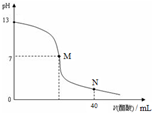 Ļņ20mL NaOHČÜŅŗÖŠÖšµĪ¼ÓČė0.1mol/L“×ĖįČÜŅŗ£¬µĪ¶ØĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
Ļņ20mL NaOHČÜŅŗÖŠÖšµĪ¼ÓČė0.1mol/L“×ĖįČÜŅŗ£¬µĪ¶ØĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
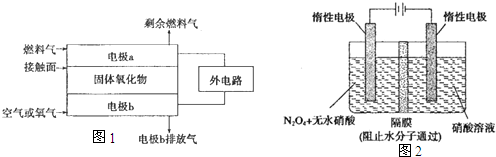
| ĻõĖį | ĻõĖįÅØ¶Č“óÓŚ10mol/L | ĻõĖįÅضČĪŖ6.6”«10mol/L”¢¼ÓČČ | ĻõĖįÅضČĪŖ6.6”«10mol/L |
| »¹Ō²śĪļ | NO2 | NO2 | NO2 |
| ĻõĖį | ĻõĖįÅضČĪŖ0.1”«6.6mol/L”¢¼ÓČČ | ĻõĖįÅضČ0.1”«6.6mol/L | ĻõĖįÅضČ0.1mol/L |
| »¹Ō²śĪļ | NO | NO2”¢N2 | NH4NO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ѧğŗžÄĻŅęŃōóšŃŌ֊ѧø߶žĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌĄķæĘ»ÆѧŹŌ¾ķ£Ø“ų½āĪö£© ĢāŠĶ£ŗµ„Ń”Ģā
Ļņ20 mL NaOHČÜŅŗÖŠÖšµĪ¼ÓČė0.1 mol/L“×ĖįČÜŅŗ£¬µĪ¶ØĒśĻßČēÓŅĶ¼ĖłŹ¾”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø £©
| A£®ŌŚMµć£¬Į½ÕßĒ”ŗĆ·“Ó¦ĶźČ« |
| B£®µĪ¶ØĒ°£¬ĖįÖŠc(H£«) µČÓŚ¼īÖŠc(OH£) |
| C£®NaOHČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ0.1 mol/L |
| D£®ŌŚNµć£¬c(CH3COO-)>c(Na+)>c(H+)>c(CH3COOH) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģɽ¶«Ź”Ī«·»ŹŠø߶žÉĻѧʌʌĩĶ³æ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø1£©25”ꏱ£¬ÅضČĪŖ0.1 mol”¤L£1µÄ6ÖÖČÜŅŗ£ŗ¢ŁHCl£¬ ¢ŚCH3OOH£¬ ¢ŪBa(OH)2£¬¢ÜNa 2CO3£¬¢ŻKCl£¬¢ŽNH4ClČÜŅŗpHÓÉŠ”µ½“óµÄĖ³ŠņĪŖ__________________(ĢīŠ“±ąŗÅ)”£
£Ø2£©25”ꏱ£¬“×ĖįµÄµēĄė³£ŹżKa=1.7”Į10-5mol/L£¬ŌņøĆĪĀ¶ČĻĀCH3COONaµÄĖ®½āĘ½ŗā³£ŹżKh= mol ”¤L-1£Ø±£Įōµ½Š”ŹżµćŗóŅ»Ī»£©”£
£Ø3£©25”ꏱ£¬pH£½3µÄ“×ĖįŗĶpH£½11µÄĒāŃõ»ÆÄĘČÜŅŗµČĢå»ż»ģŗĻŗó£¬ČÜŅŗ³Ź £ØĢī”°ĖįŠŌ”±£¬”°ÖŠŠŌ”±»ņ”°¼īŠŌ”±£© £¬ĒėŠ“³öČÜŅŗÖŠĄė×ÓÅØ¶Č¼äµÄŅ»øöµČŹ½£ŗ ”£
£Ø4£©25”ꏱ£¬½«m mol/LµÄ“×ĖįŗĶn mol/LµÄĒāŃõ»ÆÄĘČÜŅŗµČĢå»ż»ģŗĻŗó£¬ČÜŅŗµÄpH£½7£¬
ŌņČÜŅŗÖŠc(CH3COO£) + c(CH3COOH)= £¬mÓėnµÄ“󊔹ŲĻµŹĒ£ķ £ī£ØĢī”° £¾”±”°£½”±»ņ”°<”± £©”£
£Ø5£©25”ꏱ£¬½«µČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄ“×ĖįÓė°±Ė®»ģŗĻŗó£¬ČÜŅŗµÄpH£½7 £¬ŌņNH3”¤H2OµÄµēĄė³£ŹżKa= ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013½ģŗžÄĻŅęŃōóšŃŌ֊ѧø߶žĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌĄķæĘ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ļņ20 mL NaOHČÜŅŗÖŠÖšµĪ¼ÓČė0.1 mol/L“×ĖįČÜŅŗ£¬µĪ¶ØĒśĻßČēÓŅĶ¼ĖłŹ¾”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø £©

A£®ŌŚMµć£¬Į½ÕßĒ”ŗĆ·“Ó¦ĶźČ«
B£®µĪ¶ØĒ°£¬ĖįÖŠc(H£«) µČÓŚ¼īÖŠc(OH£)
C£®NaOHČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ0.1 mol/L
D£®ŌŚNµć£¬c(CH3COO-)>c(Na+)>c(H+)>c(CH3COOH)
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com