
 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素基态原子没有不成对电子;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层只有1个电子,其余各内层轨道均充满电子.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素基态原子没有不成对电子;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层只有1个电子,其余各内层轨道均充满电子.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):分析 A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn,而n=2,则A为N元素;E原子核外的M层中只有两对成对电子,外围电子排布为3s23p4,则E为S元素;化合物B2E为离子化合物,B表现+1价,原子序数大于碳、小于硫,则B为Na;C元素基态原子没有不成对电子,原子序数介于钠、硫之间,核外电子排布式为1s22s22p63s2,故C为Mg;D单质常用于制作太阳能电池和集成电路芯片,则D为Si;F原子最外层电子数与B的相同,其余各内层轨道均充满电子,原子序数大于硫,处于第四周期,核外电子数为2+8+18+1=19,则F为Cu.
解答 解:A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn,而n=2,则A为N元素;E原子核外的M层中只有两对成对电子,外围电子排布为3s23p4,则E为S元素;化合物B2E为离子化合物,B表现+1价,原子序数大于碳、小于硫,则B为Na;C元素基态原子没有不成对电子,原子序数介于钠、硫之间,核外电子排布式为1s22s22p63s2,故C为Mg;D单质常用于制作太阳能电池和集成电路芯片,则D为Si;F原子最外层电子数与B的相同,其余各内层轨道均充满电子,原子序数大于硫,处于第四周期,核外电子数为2+8+18+1=19,则F为Cu.
(1)同周期随原子序数增大第一电离能呈增大趋势,Mg原子3s轨道为全满稳定状态,能量较低,第一电离能高于同周期相邻元素的,故第一电离能:Na<Al<Mg,
故答案为:Na<Al<Mg;
(2)C2H4分子C原子形成2个C-H键、1个C-C键,没有孤对电子,碳原子杂化轨道数目为3,故碳原子采取sp2杂化,
故答案为:sp2;
(3)F为Cu,处于周期表中第四周期第IB族,H2S通入Cu2+水溶液反应的离子方程式为:Cu2++H2S=CuS↓+2H+,
故答案为:第四周期第IB族;Cu2++H2S=CuS↓+2H+;
(4)碳和Al可形成一种新型化合物材料,其晶体具有很高的硬度和熔点,该化合物属于原子晶体,化合物中所含的化学键类型为共价单键,属于σ 键;
A、D的最高价氧化物分别为CO2、SiO2,前者属于分子晶体,后者属于原子晶体,故CO2低于SiO2,
故答案为:σ 键;CO2<SiO2;CO2属于分子晶体,微粒间以范德华力结合,SiO2属于原子晶体,微粒间以共价键结合;
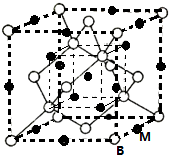
(5)与B同主族原子半径最小的元素M为H,晶胞中H原子数目为5+12×$\frac{1}{4}$=8,Na原子数目为4+8×$\frac{1}{8}$+6×$\frac{1}{2}$=8,故晶体化学式为NaH,
晶胞质量为8×$\frac{24}{{N}_{A}}$g,距离最近的两个B、M原子的核间距为a nm,则晶胞棱长为2a nm,则该化合物的晶胞密度为8×$\frac{24}{{N}_{A}}$g÷(2a×10-7 cm)3=$\frac{24×1{0}^{21}}{{a}^{3}×{N}_{A}}$g/cm3,
故答案为:NaH;$\frac{24×1{0}^{21}}{{a}^{3}×{N}_{A}}$.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、电离能、杂化方式、化学键、晶体类型与性质、晶胞计算等,推断元素是解题关键,需要学生具备扎实的基础与灵活运用能力,注意同周期主族元素中第一电离能异常原因.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 2-甲基-3-乙基戊烷 | B. | 3,4,4-三甲基己烷 | ||
| C. | 2-甲基-4-乙基戊烷 | D. | 1,2-二甲基丁烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液态水的密度大于冰的密度 | B. | 碘单质和干冰容易升华 | ||
| C. | 氧气的氧化性不如氯气的氧化性 | D. | 溴容易溶于四氯化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 原子序数 | 核外电子排布式 | 外围电子排布式 | 周期表中的位置 |
| 16 | 1S22S22P63S23P4 | 3s23p4 | 第三周期第ⅥA族 |
| 23 | 1S22S22P63S23P63d34s2 | 3d34s2 | 第四周期第ⅤB族 |
| 34 | 1S22S22P63S23P63d104s24p4 | 4s24p4 | 第四周期第ⅥA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 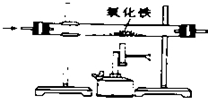 除去CO中的CO2 除去CO中的CO2 | B. | 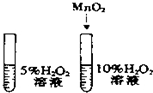 探究二氧化锰对反应速率的影响 探究二氧化锰对反应速率的影响 | ||
| C. | 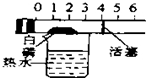 探究空气中氧气的含量 探究空气中氧气的含量 | D. | 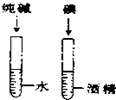 探究溶解性的影响因素 探究溶解性的影响因素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
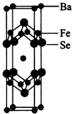 不锈钢是一种常见的合金,耐高温,加工性能好,在生产生活中有广泛用途.一种不锈钢的主要成分是Fe、Ni、Cr、Si、P.回答下列问题:
不锈钢是一种常见的合金,耐高温,加工性能好,在生产生活中有广泛用途.一种不锈钢的主要成分是Fe、Ni、Cr、Si、P.回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
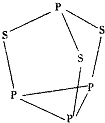 有A、B、C、D、E五种元素.其相关信息如下:
有A、B、C、D、E五种元素.其相关信息如下:| 元素 | 相关信息 |
| A | A元素的一种原子没有中子,只有一个质子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道有三个未成对电子 |
| D | D为主族元素,且与E同周期,其最外层上有两个运动状态不同的电子 |
| E | E能形成砖红色(红色)的E2O和EO两种氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
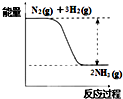 在已经发现的一百多种元素中,除稀有气体外,非金属元素只有十多种,但与生产生活有密切的联系.
在已经发现的一百多种元素中,除稀有气体外,非金属元素只有十多种,但与生产生活有密切的联系.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com