
| A. | K+、MnO4-、Cl-、SO42- | B. | Na+、AlO2-、Cl-、SO42- | ||
| C. | SO42-、Fe3+、HCO3-、Ba2+ | D. | Mg2+、NO3-、NH4+、SO42- |
分析 碱性溶液中含大量的氢氧根离子,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应、水解等,则离子大量共存,并结合离子的颜色来解答.
解答 解:A.MnO4-为紫色,与无色不符,故A不选;
B.碱性溶液中该组离子之间不反应,可大量共存,且离子均为无色,故B选;
C.Fe3+、HCO3-相互促进水解,SO42-、Ba2+结合生成沉淀,不能共存,故C不选;
D.碱性溶液中不能大量存在Mg2+、NH4+,故D不选;
故选B.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、水解反应的判断,题目难度不大.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 3s2表示3s能级有两个轨道 | |
| B. | 处于最低能量的原子叫做基态原子 | |
| C. | 同一原子中,1s、2s、3s电子的能量逐渐减小 | |
| D. | 同一原子中,3d、4d、5d能级的轨道数依次增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌为电池负极,发生氧化反应 | |
| B. | 电池工作时,氧气与锌直接化合,生成氧化锌 | |
| C. | 正极发生的反应是:$\frac{1}{2}$O2+2e-+2H+═H2O | |
| D. | 负极发生的反应是:Zn-2e-+H2O═ZnO+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
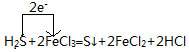 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
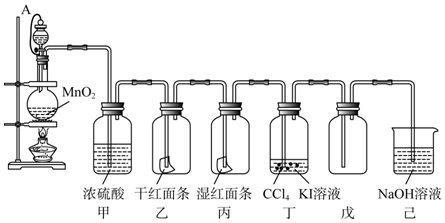
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 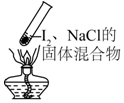 加热时,上部汇聚了固体碘,说明碘的热稳定性较差 | |
| B. | 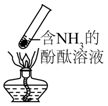 加热时,中部溶液变红,冷却后又变为无色 | |
| C. | 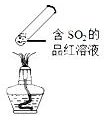 加热时,中部溶液变红,冷却后又变为无色 | |
| D. |  \加热时,上部汇聚了白色固体,说明氯化铵易升华 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
| 编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/ml | 100mL | 200mL | 300mL | 400mL |
| 剩余金属/g | 18.0g | 9.6g | 0 | 0 |
| NO体积/L | 2.24L | 4.48L | 6.7L | V |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
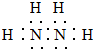 ,HCN中C的化合价为-2.
,HCN中C的化合价为-2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com