
 ,H为桂皮酸甲酯的一种同分异构体,而桂皮酸的苯环上只有一个取代基,结合H的结构简式可知,桂皮酸的结构简式为
,H为桂皮酸甲酯的一种同分异构体,而桂皮酸的苯环上只有一个取代基,结合H的结构简式可知,桂皮酸的结构简式为 ,则桂皮酸甲酯为
,则桂皮酸甲酯为 .G与甲醇发生酯化反应生成H,则G为
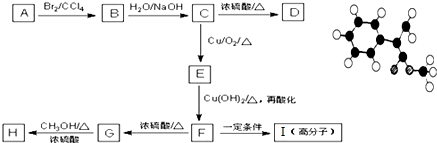
.G与甲醇发生酯化反应生成H,则G为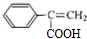 ,A与溴的四氯化碳溶液反应生成B,B发生卤代烃的水解反应反应生成C,C氧化生成E,E进一步氧化、酸化得到F,F在浓硫酸、加热条件下生成G,应是发生消去反应,由G的结构可知,A为
,A与溴的四氯化碳溶液反应生成B,B发生卤代烃的水解反应反应生成C,C氧化生成E,E进一步氧化、酸化得到F,F在浓硫酸、加热条件下生成G,应是发生消去反应,由G的结构可知,A为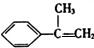 ,则B为
,则B为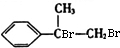 ,C为
,C为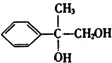 ,E为
,E为 ,F为
,F为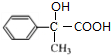 ,F发生缩聚反应生成I为
,F发生缩聚反应生成I为 ,C在浓硫酸、加热条件下发生消去反应生成D为
,C在浓硫酸、加热条件下发生消去反应生成D为 ,据此解答.
,据此解答. ,H为桂皮酸甲酯的一种同分异构体,而桂皮酸的苯环上只有一个取代基,结合H的结构简式可知,桂皮酸的结构简式为
,H为桂皮酸甲酯的一种同分异构体,而桂皮酸的苯环上只有一个取代基,结合H的结构简式可知,桂皮酸的结构简式为 ,则桂皮酸甲酯为
,则桂皮酸甲酯为 .G与甲醇发生酯化反应生成H,则G为
.G与甲醇发生酯化反应生成H,则G为 ,A与溴的四氯化碳溶液反应生成B,B发生卤代烃的水解反应反应生成C,C氧化生成E,E进一步氧化、酸化得到F,F在浓硫酸、加热条件下生成G,应是发生消去反应,由G的结构可知,A为
,A与溴的四氯化碳溶液反应生成B,B发生卤代烃的水解反应反应生成C,C氧化生成E,E进一步氧化、酸化得到F,F在浓硫酸、加热条件下生成G,应是发生消去反应,由G的结构可知,A为 ,则B为
,则B为 ,C为
,C为 ,E为
,E为 ,F为
,F为 ,F发生缩聚反应生成I为
,F发生缩聚反应生成I为 ,C在浓硫酸、加热条件下发生消去反应生成D为
,C在浓硫酸、加热条件下发生消去反应生成D为 ,
, ,故答案为:
,故答案为: ;
; ,分子中有7种化学环境不同的氢原子,故b正确;
,分子中有7种化学环境不同的氢原子,故b正确; ,羧基与碳酸钠反应,2mol有机物F与足量碳酸钠溶液反应没有CO2生成,故c错误;
,羧基与碳酸钠反应,2mol有机物F与足量碳酸钠溶液反应没有CO2生成,故c错误; ,含有苯环与醛基,可以与氢气发生加成反应,属于还原反应,醛基可以发生氧化反应,含有醇羟基,可以发生取代反应,且羟基连接的碳原子相邻碳原子上含有氢原子,可以发生消去反应,故d正确;
,含有苯环与醛基,可以与氢气发生加成反应,属于还原反应,醛基可以发生氧化反应,含有醇羟基,可以发生取代反应,且羟基连接的碳原子相邻碳原子上含有氢原子,可以发生消去反应,故d正确;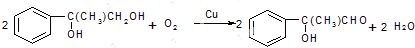 ;
;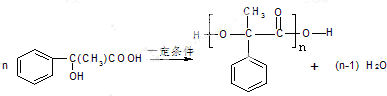 ,
,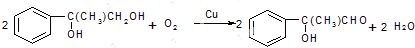 ;
; ;
; ,含有碳碳双键,醛基氧化为羧基可能同时氧化碳碳双键,最终不能有效、顺利地转化为G,
,含有碳碳双键,醛基氧化为羧基可能同时氧化碳碳双键,最终不能有效、顺利地转化为G, )的同分异构体:①遇FeCl3溶液显紫色,说明含有酚羟基;②能发生水解反应,且能发生银镜反应,含有甲酸形成的酯基;③苯环上有两个取代基,除酚羟基外,另外的取代基为-CH2CH2OOCH或-CH(CH3)OOCH,各有邻、间、对三种,共共有6种,
)的同分异构体:①遇FeCl3溶液显紫色,说明含有酚羟基;②能发生水解反应,且能发生银镜反应,含有甲酸形成的酯基;③苯环上有两个取代基,除酚羟基外,另外的取代基为-CH2CH2OOCH或-CH(CH3)OOCH,各有邻、间、对三种,共共有6种, ,
, .
.


科目:高中化学 来源: 题型:
| A、16O与18O互为同分异构体 |
| B、16O与18O核外电子排布不同 |
| C、通过化学变化可以实现16O与18O间的转化 |
| D、标准状况下,1.12L 16O2和1.12L18O2均含有0.1NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
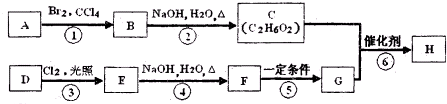
查看答案和解析>>
科目:高中化学 来源: 题型:
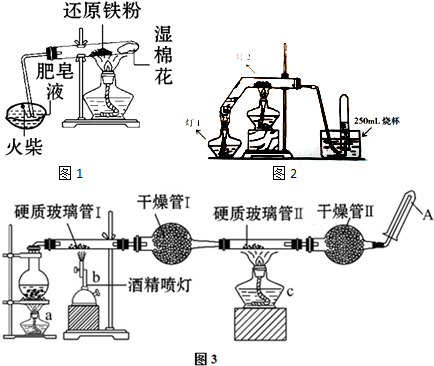
查看答案和解析>>
科目:高中化学 来源: 题型:
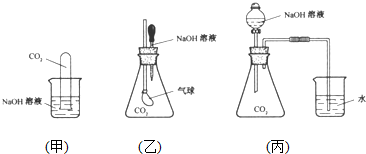
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCO3- |
| B、Na+ |
| C、Ba2+ |
| D、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 | 0.4 |
| 3 | 4 |
| 3 | 6 |
| 3 | 60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHS水解反应:HS-+H2O═H3O++S2- | ||||
B、少量铁与热的浓硝酸反应:Fe+6HNO3(浓)
| ||||
C、 如图装置中石墨电极上的电极反应为:O2+4e-+2H2O=4OH- | ||||
D、湿法炼铜的原理:Cu2S+O2
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com