
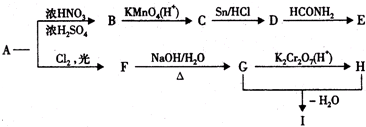
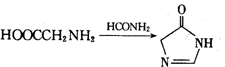
 ,物质E含2个六元环.
,物质E含2个六元环. ,则C通过信息反应②转化成D,则C为
,则C通过信息反应②转化成D,则C为 ;B被酸性高锰酸钾溶液氧化成C,则B的结构简式为:
;B被酸性高锰酸钾溶液氧化成C,则B的结构简式为: ;A与浓硝酸在浓硫酸存在条件下发生硝化反应生成B,A的相对分子质量为92,则A为
;A与浓硝酸在浓硫酸存在条件下发生硝化反应生成B,A的相对分子质量为92,则A为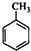 ;D通过信息反应③生成E,E含有2个六元环,则E的结构简式为:
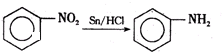
;D通过信息反应③生成E,E含有2个六元环,则E的结构简式为: ;A与氯气在光照条件下生成F,则F为
;A与氯气在光照条件下生成F,则F为 ,F发生水解生成G,则G为
,F发生水解生成G,则G为 ,苯甲醇被酸性重铬酸钾溶液氧化成H,则H为苯甲酸,苯甲酸与苯甲醇发生酯化反应生成I,反应的方程式为:
,苯甲醇被酸性重铬酸钾溶液氧化成H,则H为苯甲酸,苯甲酸与苯甲醇发生酯化反应生成I,反应的方程式为: ,据此进行解答.
,据此进行解答. ,则C通过信息反应②转化成D,则C为
,则C通过信息反应②转化成D,则C为 ;B被酸性高锰酸钾溶液氧化成C,则B的结构简式为:
;B被酸性高锰酸钾溶液氧化成C,则B的结构简式为: ;A与浓硝酸在浓硫酸存在条件下发生硝化反应生成B,A的相对分子质量为92,则A为
;A与浓硝酸在浓硫酸存在条件下发生硝化反应生成B,A的相对分子质量为92,则A为 ;D通过信息反应③生成E,E含有2个六元环,则E的结构简式为:
;D通过信息反应③生成E,E含有2个六元环,则E的结构简式为: ;A与氯气在光照条件下生成F,则F为
;A与氯气在光照条件下生成F,则F为 ,F发生水解生成G,则G为
,F发生水解生成G,则G为 ,苯甲醇被酸性重铬酸钾溶液氧化成H,则H为苯甲酸,苯甲酸与苯甲醇发生酯化反应生成I,反应的方程式为:
,苯甲醇被酸性重铬酸钾溶液氧化成H,则H为苯甲酸,苯甲酸与苯甲醇发生酯化反应生成I,反应的方程式为: ,
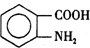
, ,其分子中含有羧基和硝基,
,其分子中含有羧基和硝基, ,苯甲醇中含有羟基,能够与钠反应生成氢气,能够与溴化氢发生取代反应,能够与乙酸发生酯化反应,但是不能与碳酸钠反应,故abd正确、c错误,
,苯甲醇中含有羟基,能够与钠反应生成氢气,能够与溴化氢发生取代反应,能够与乙酸发生酯化反应,但是不能与碳酸钠反应,故abd正确、c错误, ;I为苯甲醇与苯甲酸发生酯化反应生成的苯甲酸苯甲酯,
;I为苯甲醇与苯甲酸发生酯化反应生成的苯甲酸苯甲酯, ; 苯甲酸苯甲酯;
; 苯甲酸苯甲酯; ,
, ;
; ,①属于芳香族化合物,说明分子中含有苯环;②可以发生银镜反应,分子中含有醛基,则满足条件的且与H互为同分异构体的有机物为的结构简式为:
,①属于芳香族化合物,说明分子中含有苯环;②可以发生银镜反应,分子中含有醛基,则满足条件的且与H互为同分异构体的有机物为的结构简式为: 、
、 、
、 、
、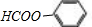 ,总共有4种;
,总共有4种; 分子中含有6种等效H原子、
分子中含有6种等效H原子、 中含有6种等效H原子、
中含有6种等效H原子、 中含有4种等效H原子、
中含有4种等效H原子、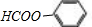 中含有4种等效H原子,等效H原子的数目决定的了核磁共振氢谱中峰的种类,所以核磁共振氢谱中最多出现6种峰,
中含有4种等效H原子,等效H原子的数目决定的了核磁共振氢谱中峰的种类,所以核磁共振氢谱中最多出现6种峰,

科目:高中化学 来源: 题型:
| A、溶液中NH4+和OH-在加热时可生成NH3 |
| B、铵盐受热分解均有生成NH3放出 |
| C、铵盐均易溶于水 |
| D、铵盐属于离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-) |
| B、NaHSO4 溶液:c(H+)=c(SO42-)+c(OH-) |
| C、pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中c(Cl-)>c(H+)>c(NH4+ )>c(OH-) |
| D、Na2S溶液:c(Na+ )=2c(HS-)+2c(S2-)>2c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
| 第三次 | 10.00 | 0.40 | 23.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5种 | B、6种 | C、8种 | D、9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、因浓硫酸具有强氧化性,故不可用它来干燥氢气 |
| B、浓硫酸与浓氨水靠近时产生大量白烟 |
| C、浓硫酸有强氧化性,稀硫酸不具有氧化性 |
| D、浓硫酸具有腐蚀性,取用时要小心 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com