
 zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是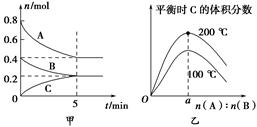
 zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2 C(g)。200℃时,A、B、C的平衡浓度分别是0.2mol/L、0.1mol/L、0.1mol/L,根据化学平衡常数的定义得K=0.1mol/L/0.1mol/L×(0.2mol/L)2="25" L2/mol2,正确;C、当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均减小,错误;D、由图乙可知温度升高,C的体积分数增大,说明升高温度,平衡正向移动,正向为吸热反应,ΔH>0,a值不确定,错误,答案选B。
C(g)。200℃时,A、B、C的平衡浓度分别是0.2mol/L、0.1mol/L、0.1mol/L,根据化学平衡常数的定义得K=0.1mol/L/0.1mol/L×(0.2mol/L)2="25" L2/mol2,正确;C、当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均减小,错误;D、由图乙可知温度升高,C的体积分数增大,说明升高温度,平衡正向移动,正向为吸热反应,ΔH>0,a值不确定,错误,答案选B。

科目:高中化学 来源:不详 题型:填空题
 2NO2(g) ΔH="+57.20kJ" · mol-1
2NO2(g) ΔH="+57.20kJ" · mol-1| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4) /mol··L-1 | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2) /mol·L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
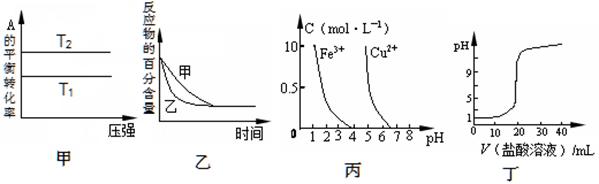
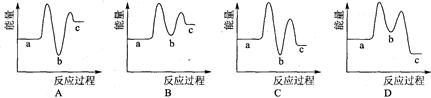
A.由图甲可以判断:若T1>T2,反应A(g)+ B(g) 2C(g)的△H<0 2C(g)的△H<0 |
B.图乙表示压强对可逆反应2A(g)+2 B(g) 3C(g)+D(s)的影响,乙的压强比甲的压强大 3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| C.根据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量NaOH溶液,调节pH≈4 |
| D.图丁表示用0.1mol/L的盐酸滴定20mL 0.1mol/LNaOH溶液,溶液pH随加入盐酸体积的变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2PbCrO4(s)+2H+(aq)△H<0
2PbCrO4(s)+2H+(aq)△H<0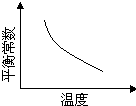
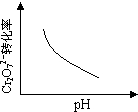
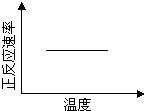
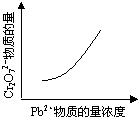
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 CO(NH2)2(l)+H2O(l)
CO(NH2)2(l)+H2O(l)  ,该反应在 (填“较高温度”或“较低温度”)下能自发进行。
,该反应在 (填“较高温度”或“较低温度”)下能自发进行。 NH2COONH4(s)
NH2COONH4(s) 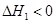
 CO(NH2)2(l)+ H2O(l)
CO(NH2)2(l)+ H2O(l) 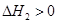
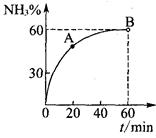
 物质 物质n/mol T/℃ | 活性炭 | NO | E | F |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等压时,通入惰性气体,c的物质的量不变 |
| B.等压时,通入z气体,反应器中温度升高 |
| C.等容时,通入惰性气体,各反应速率不变 |
| D.等容时,通入z气体,y的物质的量浓度增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
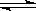 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )| A.Z为0.3mol/L | B.Y2为0.4mol/L | C.X2为0.2mol/L | D.Z为0.4mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2AB(g)达到平衡的标志是 ( )
2AB(g)达到平衡的标志是 ( )| A.单位时间内消耗n mol A2同时生成2n mol AB |
| B.容器内的总物质的量不随时间变化 |
| C.单位时间内生成2n mol AB的同时生成n mol B2 |
| D.单位时间内生成n molA2的同时生成n mol B2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C2H5OH + 3H2O的数据如下图所示。
C2H5OH + 3H2O的数据如下图所示。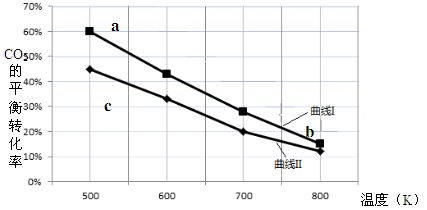

| A.该反应的△H > 0 |
| B.达平衡时,v(H2)正 = v(CO2)逆 |
| C.b点对应的平衡常数K值大于c点 |
| D.a点对应的H2的平衡转化率为90 % |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com