
ŅŃÖŖ£ŗijĪĀ¶ČŹ±£¬KW=1.0”Į10£12”£ŌŚøĆĪĀ¶ČĻĀ,²āµĆ0.1mol”¤L£1Na2AČÜŅŗPH=6,ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®H2AŌŚĖ®ČÜŅŗÖŠµÄµēĄė·½³ĢŹ½ĪŖ£ŗH2A=H++HA-£¬HA£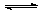 H++A2-
H++A2-
B£®³£ĪĀĻĀ£¬NH4HAČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗÖĮČÜŅŗpH=7£¬Ōņc(Na+) = 2c(A2£)
C£®ĻąĶ¬Ģõ¼žĻĀ£¬Ģå»żĻąµČ”¢pHĻąµČµÄŃĪĖįÓėH2AČÜŅŗÖŠŗĶNaOHµÄĮæĻąµČ
D£®0.0l mol”¤L-lµÄNaHAČÜŅŗpH£¾2

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖŌśÄĒĆ×Ī¤ŹĒĮ÷øŠ²”¶¾Éń¾°±ĖįĆøŅÖÖĘ¼Į£¬Ęä¶ŌĮ÷øŠ²”¶¾µÄŅÖÖĘŹĒŅŌ»ŗĀż½įŗĻµÄ·½Ź½
½ųŠŠµÄ£¬¾ßÓŠø߶ČĢŲŅģŠŌ£¬Ęä·Ö×Ó½į¹¹ČēĻĀĖłŹ¾”£
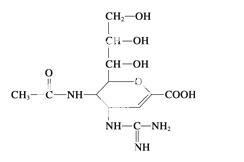
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ (””””)
A£®øĆĪļÖŹµÄ·Ö×ÓŹ½ĪŖC12H20N4O7
B£®1 moløĆĪļÖŹÓėNaOHČÜŅŗ·“Ó¦£¬æÉŅŌĻūŗÄ4 mol NaOH
C£®ŌŚŅ»¶ØĢõ¼žĻĀ£¬øĆĪļÖŹæÉŅŌ·¢ÉśĻūČ„”¢¼Ó³É”¢Č”“śµČ·“Ó¦
D£®øĆĪļÖŹÄÜŹ¹äåĖ®»ņĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£¬ÄÜÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĪļÖŹ»„ĪŖĶ¬·ÖŅģ¹¹ĢåµÄŹĒ(””””)
A£®µķ·ŪŗĶĻĖĪ¬ĖŲ
B£®øŹ°±ĖįŗĶĻõ»łŅŅĶé
C£®“×ĖįŗĶÓ²Ö¬Ėį
D£®¼×“¼ŗĶ¶ž¼×ĆŃ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀĻĀ£¬¶ŌpH=10µÄNaHCO3ČÜŅŗÖŠ£¬ø÷Ī¢Į£µÄĪļÖŹµÄĮæÅØ¶Č·ÖĪöÕżČ·µÄŹĒ£Ø £©
A£®c(CO32—)£¾c(H2CO3)
B£®c(Na£«)£¾c(HCO3—)£¾c(OH”Ŗ)£¾c(H£«)
C£®c(Na£«)£«c(H£«)£½c(HCO3—)£«c(CO32—)£«c(OH”Ŗ)
D£®c(Na£«)£½c(HCO3—)£«c(CO32—)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ(”” ””)
A£®ŹµŃéŹŅÖĘĒāĘų£¬ĪŖĮĖ¼Óæģ·“Ó¦ĖŁĀŹ£¬æÉĻņĻ”H2SO4ÖŠµĪ¼ÓÉŁĮæCu£ØNO3£©2ČÜŅŗ
B£®ĪŖ“¦Ąķ¹ųĀÆĖ®¹øÖŠµÄCaSO4£¬æÉĻČÓƱ„ŗĶNa2CO3ČÜŅŗ½žÅŻ£¬ŌŁ¼ÓČėŃĪĖįČܽā
C£®N2(g)£«3H2(g) 2NH3(g) ¦¤H£¼0£¬ĘäĖūĢõ¼ž²»±äŹ±ÉżøßĪĀ¶Č£¬Ę½ŗāŹ±ĒāĘų×Ŗ»ÆĀŹŌö“ó
2NH3(g) ¦¤H£¼0£¬ĘäĖūĢõ¼ž²»±äŹ±ÉżøßĪĀ¶Č£¬Ę½ŗāŹ±ĒāĘų×Ŗ»ÆĀŹŌö“ó
D£®ĪüČČ·“Ó¦”°TiO2£Øs£©£«2Cl2£Øg£©£½TiCl4£Øg£©£«O2£Øg£©”±ŌŚŅ»¶ØĢõ¼žĻĀæÉ×Ō·¢½ųŠŠ£¬ŌņøĆ·“Ó¦µÄ¦¤S£¼0
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓÉĮāĆ¾æó(Ö÷ŅŖ³É·ÖĪŖMgCO3)ÖĘ×čČ¼ŠĶĒāŃõ»ÆĆ¾µÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
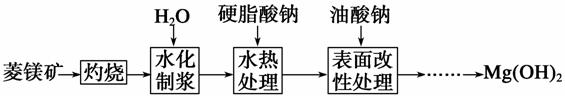
(1)“ÓĶ¼1ŗĶĶ¼2æÉŅŌµĆ³öµÄ½įĀŪĪŖ__________________”¢____________________”£
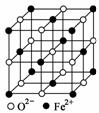
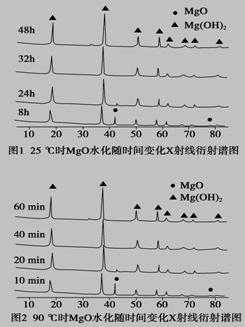
(2)Ė®»Æ·“Ó¦MgO£«H2O===Mg(OH)2ÄÜ×Ō·¢½ųŠŠµÄŌŅņŹĒ____________________”£
(3)½įŗĻŌŖĖŲÖÜĘŚĀÉŗĶĻĀ±ķæÉÖŖ£¬½šŹōĒāŃõ»ÆĪļŹÜČČ·Ö½āµÄ¹ęĀÉÓŠ__________________”£(Š“Ņ»Ģõ¼“æÉ)
²æ·ÖÖ÷×åŌŖĖŲµÄ½šŹōĒāŃõ»ÆĪļČČ·Ö½āĪĀ¶Č/”ę
| LiOH | NaOH | KOH | Al(OH)3 | Mg(OH)2 | Ca(OH)2 | Ba(OH)2 |
| 924 | ²»·Ö½ā | ²»·Ö½ā | 140 | 258 | 390 | 700 |
(4)ŅŃÖŖČČ»Æѧ·½³ĢŹ½£ŗMg(OH)2(s)===MgO(s)£«H2O(g)””¦¤H£½£«81.5 kJ”¤mol£1
¢ŁMg(OH)2Ęš×čČ¼×÷ÓƵÄÖ÷ŅŖŌŅņŹĒ________________________________________
________________________________________________________________________ӣ
¢ŚÓė³£ÓĆĀ±Ļµ(ČēĖÄäåŅŅĶé)ŗĶÓŠ»śĮ×Ļµ(Į×ĖįČż±½õ„)×čČ¼¼ĮĻą±Č£¬Mg(OH)2×čČ¼¼ĮµÄÓŵćŹĒ____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
øųĻĀĮŠ±½µÄĶ¬ĻµĪļĆüĆū
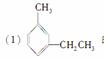 µÄĻµĶ³Ćū³ĘĪŖ
µÄĻµĶ³Ćū³ĘĪŖ
________________________________________________________________________ӣ
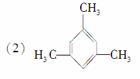 µÄĻµĶ³Ćū³ĘĪŖ
µÄĻµĶ³Ćū³ĘĪŖ
________________________________________________________________________ӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£®Ä³ĒæŃõ»Æ¼ĮXO(OH)2+±»Na2SO3»¹Ō”£Čē¹ū»¹Ō2.4”Į10-3mol XO(OH)2+£¬ŠčÓĆ30mL 0.2mol/LµÄNa2SO3ČÜŅŗ£¬ÄĒĆ“XŌŖĖŲ±»»¹ŌŗóµÄ¼ŪĢ¬ŹĒ
A.+2 B.+1 C.0 D.-1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
æĘ¼¼¹¤×÷ÕßĢį³öÓĆĀĮ·Ū“¦Ąķŗ¬ŃĒĻõĖįŃĪ·ĻĖ®µÄĖ¼Ā·£ŗµ÷½ŚŃĒĻõĖįŃĪ·ĻĖ®Ėį¼īŠŌ£¬Ź¹ĘäpH>12£¬Č»ŗó¼ÓČėŹŹĮæµÄĀĮ·Ū”¢½Į°č£¬“Ó¶ųŹµĻÖŌ¤ĘŚÄæµÄ”£ĻĀĮŠÅŠ¶Ļ“ķĪóµÄŹĒ
””A£®·ĻĖ®“¦ĄķŹ±ĀĮµ„ÖŹ×Ŗ»ÆĪŖAl3+””B£®·ĻĖ®“¦ĄķÖŠ£¬ŃĒĻõĖįŃĪ±»»¹Ō
””C£®“¦Ąķ¹ż³ĢÖŠ£¬OHŅ»²ĪÓėĮĖ·“Ó¦””D£®ĀĮ·ŪæÅĮ£“óŠ”Ó°Ļģ·ĻĖ®“¦ĄķµÄĖŁĀŹ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com