
某化学反应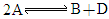 在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(
在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(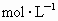 )随反应时间(min)的变化情况见下表.
)随反应时间(min)的变化情况见下表.
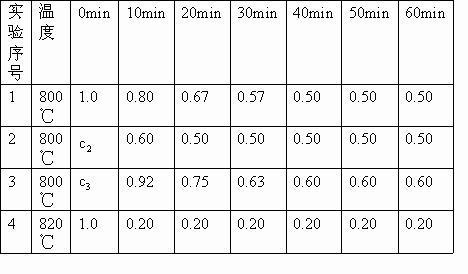
根据上述数据,完成下列填空:
(1)在实验1中,反应在10至20min时间内平均速率为_________ .
.
(2)在实验2中,A的初始浓度 =________
=________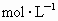 ,反应经20min就达到平衡,可推测实验2中还隐含的条件是________.
,反应经20min就达到平衡,可推测实验2中还隐含的条件是________.
(3)设实验3的反应速率为 ,实验1的反应速率为
,实验1的反应速率为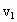 ,则
,则 ________
________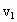 (填“>”=”或“<”),且
(填“>”=”或“<”),且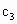 ________1.0
________1.0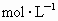 (填“>”“=”或“<”).
(填“>”“=”或“<”).
(4)比较实验4和实验1,可推测该反应是________反应(填“吸热”“放热”).理由是_______________________.
|
答案: (1)0.013 (2)1.0;使用催化剂 (3)>;> (4)吸热;温度升高时,平衡向右移动解析: (1)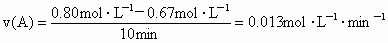
(2) 对比实验1与实验2可知,反应温度相同,达平衡时A的浓度相同,说明是同一平衡状态,即 ,又因实际反应的速率快,达平衡所需时间短,说明反应中使用了催化剂. ,又因实际反应的速率快,达平衡所需时间短,说明反应中使用了催化剂.
(3) 对比实验3与实验1可知,从10min到20min,实验1的A的浓度变化值为0.13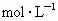 ,而实验3的A的浓度变化值为0.17 ,而实验3的A的浓度变化值为0.17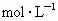 ,这就说明了 ,这就说明了 > > .又知从0min到10minA的浓度的变化值应大于0.17 .又知从0min到10minA的浓度的变化值应大于0.17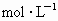 ,即 ,即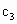 >(0.92+0.17) >(0.92+0.17)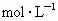 =1.09 =1.09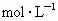 .(4)对比实验4与实验1可知,两实验的起始浓度相同,反应温度不同,达平衡时实验4的A的浓度小,说明了实验4进行得程度大,即温度越高,A的转化率越大,说明反应为吸热反应. .(4)对比实验4与实验1可知,两实验的起始浓度相同,反应温度不同,达平衡时实验4的A的浓度小,说明了实验4进行得程度大,即温度越高,A的转化率越大,说明反应为吸热反应. |


科目:高中化学 来源: 题型:
 B+D在四种不同条件下进行,B、D起始浓度为零.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为零.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:| 实验序号 | 时间/浓度/温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 B+D在四种不同条件下进行,B、D起始浓度为0及反应A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0及反应A的浓度(mol/L)随反应时间(min)的变化情况如下表:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 序号 |
温度 | 0min | 10min | 20min | 30min | 40min | 50min | 60min |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:022
(2003·上海)某化学反应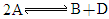 在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(
在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度( )随反应时间(min)的变化情况见下表.
)随反应时间(min)的变化情况见下表.

根据上述数据,完成下列填空:
(1)在实验1中,反应在10min至20min时间内平均速率为_________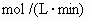 .
.
(2)在实验2,A的初始浓度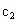 =________
=________ ,反应经20min就达到平衡,可推测实验2中还隐含的条件是___________________________.
,反应经20min就达到平衡,可推测实验2中还隐含的条件是___________________________.
(3)设实验3的反应速率为 ,实验1的反应速率为
,实验1的反应速率为 ,则
,则 ________
________ (填“>”“=”或“<”),且
(填“>”“=”或“<”),且 ________1.0
________1.0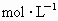 (填“>”“=”或“<”).
(填“>”“=”或“<”).
(4)比较实验4和实验1,可推测该反应是________反应(填“吸热”或“放热”).理由是_______________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com