

图1-6-7
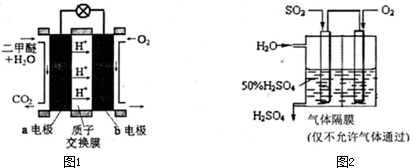
(1)左、右储罐中的电解质分别为:左____________,右____________。
(2)写出电池充电时,阳极和阴极的电极反应式。
阳极:________________________________________________,
阴极:________________________________________________。
(3)写出电池充、放电的反应方程式:________________________。
(4)指出在充电过程中钠离子通过膜的流向:________________________。
解析:能源问题是当今社会焦点问题,同时也是高考命题的热点。本题以一种燃料电池的工作原理为背景来命题,主要考查化学能如何转变成电能的知识。解答此题要求考生具有扎实的电化学知识将所学知识与现实问题综合起来分析的能力。
根据题中参加反应的物质与生成物中S与Br元素的价态在反应前后的变化,判断在原电池中正极或负极上发生反应的物质。NaBr3→NaBr(Br的价态由![]() →-1,化合价降低),Na2S2→Na2S4(S的价态由-1→
→-1,化合价降低),Na2S2→Na2S4(S的价态由-1→![]() ,化合价升高)。
,化合价升高)。
答案:(1)左:NaBr3/NaBr、左:Na2S2/Na2S4(只写一种也可)
(2)阳极:3NaBr-2e-====NaBr3+2Na+
阴极:Na2S4+2Na++2e-====2Na2S2
(3)2Na2S2+NaBr3![]() Na2S4+3NaBr
Na2S4+3NaBr
(4)充电时,左电极作阳极,右电极作阴极,故Na+的流向为从左到右


科目:高中化学 来源: 题型:阅读理解

| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 1.容器 | 2.甲 | 3.乙 | 4.丙 |
| 5.反应物投入量 | 6.1molCO、2molH2 | 7.l molCH3OH | 8.2molCO、4molH2 |
| 9.CH30H昀浓度(mol/L) | 10.cl | 11.c2 | 12.c3 |
| 13.反应的能量变化 | 14.放出Q1kJ | 15.吸收Q2kJ | 16.放出Q3kJ |
| 17.平衡常数 | 18.Kl | 19.K2 | 20.K3 |
| 21.反应物转化率 | 22.al | 23.a2 | 24.a3 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数 (K) |
7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 |
3.0×10-8 |
 ,下列说法正确的是
,下列说法正确的是 SO2Cl2(l)△H=-97.3kJ?mol-1
SO2Cl2(l)△H=-97.3kJ?mol-1查看答案和解析>>
科目:高中化学 来源:2015届河北冀州中学高二上学期第四次月考化学试卷(解析版) 题型:实验题
正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。

发生的反应如下:
CH3CH2CH2CH2OH CH3CH2CH2CHO
CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
|
|
沸点/。c |
密度/(g·cm-3) |
水中溶解性 |
|
正丁醇 |
11.72 |
0.8109 |
微溶 |
|
正丁醛 |
75.7 |
0.8017 |
微溶 |
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90—95℃,在E中收集90℃以下的馏分。
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75—77℃馏分,产量2.0g。
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,并说明理由 。
(2)加入沸石的作用是 。若加热后发现未加沸石,应采取的正确方法是 。
(3)上述装置图中,B仪器的名称是 ,D仪器的名称是 。
(4)分液漏斗使用前必须进行的操作是 (填正确答案标号)。
a.润湿 b.干燥 c.检漏 d.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在 层(填“上”或“下”)
(6)反应温度应保持在90—95℃,其原因是 。
(7)本实验中,正丁醛的产率为 %。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com