
 =
=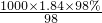 =18.4 mol/L,配制1mol/L的稀硫酸100mL,需要浓硫酸的体积为V═
=18.4 mol/L,配制1mol/L的稀硫酸100mL,需要浓硫酸的体积为V═ =0.0054L,即5.4mL,应选择10mL量筒,实验时用10mL量筒量取5.4mL浓硫酸,因配制一定物质的量浓度的溶液需要量取、溶解、移液、洗涤、定容、摇匀等操作,量取时用量筒和胶头滴管,溶解时用烧杯和玻璃棒,移液时用玻璃棒和容量瓶,定容时用胶头滴管.所以正确顺序为③②⑥⑦⑤⑥,故选A.
=0.0054L,即5.4mL,应选择10mL量筒,实验时用10mL量筒量取5.4mL浓硫酸,因配制一定物质的量浓度的溶液需要量取、溶解、移液、洗涤、定容、摇匀等操作,量取时用量筒和胶头滴管,溶解时用烧杯和玻璃棒,移液时用玻璃棒和容量瓶,定容时用胶头滴管.所以正确顺序为③②⑥⑦⑤⑥,故选A.

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容量瓶、13.6 mL量筒 | B、500 mL容量瓶、100 mL量筒 | C、容量瓶、100 mL量筒 | D、500 mL容量瓶、25 mL量筒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com