
下列说法中,正确的是
A.易溶于水的电解质一定是强电解质
B.难溶于水的电解质一定是弱电解质
C.弱电解质在水溶液中的电离过程是可逆的
D.强电解质水溶液的导电能力一定比弱电解质的强
科目:高中化学 来源: 题型:
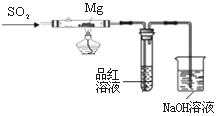 某兴趣小组依据CO2+2Mg=2MgO+C,推测Mg与SO2在隔绝空气条件下反应后,剩余固体M可能含有MgO、S、MgS、Mg中的一种或几种。为了验证推测,进行以下实验。请回答有关问题。
某兴趣小组依据CO2+2Mg=2MgO+C,推测Mg与SO2在隔绝空气条件下反应后,剩余固体M可能含有MgO、S、MgS、Mg中的一种或几种。为了验证推测,进行以下实验。请回答有关问题。
实验Ⅰ 按右图所示进行实验。
(1)实验前需除去镁条表面氧化膜。用简易的物理
方法除氧化膜的操作是 ;
(2)实验室制取二氧化硫的化学方程式为 ;
(3)上述装置存在不合理之处,请提出1项改进建议 ;
 (4)实验时,先通入SO2直到 现象出现后,再点燃酒精灯;此操作目的是 。
(4)实验时,先通入SO2直到 现象出现后,再点燃酒精灯;此操作目的是 。
实验Ⅱ 确定固体M的成分。
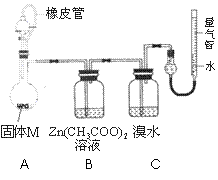
实验装置如右图所示。将分液漏斗中稀硫酸(足量)
加入到烧瓶中,完全反应后,实验现象如下:
|
(5)实验时,B装置中反应的化学方程式为 ;
(6)已知镁的相对原子质量为24,则固体M中金属镁的质量为 g;实验前装置内有空气,对金属镁质量的测定结果的影响是 (填偏低、偏高、无影响);
(7)依以上实验,可确定固体M的成分有 种(填数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
SO2和Cl2均是常用的漂白剂,若将SO2和Cl2等物质的量混合后,先缓慢通入到BaCl2溶液中,再滴入品红试液,会观察到的现象是( )
A. 无沉淀生成,溶液显红色 B. 无沉淀生成,溶液显无色
C. 有沉淀生成,溶液显无色 D. 有沉淀生成,溶液显红色
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,用化学符号回答下列有关问题:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
| |
(1)写出下列元素的符号:①_____,⑥_____,⑦_____。
(2)在这些元素中,最活泼的金属元素是____,最活泼的非金属元素是____,最不活泼的元素是____。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是_______,碱性最强的是_____,称为两性氢氧化物的是_________。
(4)在这些元素中,原子半径最小的是____,原子半径最大的是_____。
(5)在③与④,化学性质较活泼的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关环境保护的说法中错误的是
A.含氮、磷化合物的生活污水大量排放可使水体富营养化
B.各国工业大量排放二氧化硫是全球气候变暖的主要原因
C.劣质装修材料中的甲醛、苯、氡气等对人体有害
D.废旧电池中的汞、镉、铅等重金属盐对土壤和水源会造成污染
查看答案和解析>>
科目:高中化学 来源: 题型:
已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,要使溶液中c(H+)值增大,可以采取的措施是
CH3COO-+H+,要使溶液中c(H+)值增大,可以采取的措施是
A.加少量烧碱溶液 B.加蒸馏水
C.加少量醋酸钠固体 D.升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
向Cr2(SO4) 3的水溶液中,加入NaOH溶液,当pH=4.6时,开始出现Cr(OH)3沉淀,随着pH的升高,沉淀增多,但当pH≥13时,沉淀消失,出现亮绿色的亚铬酸根离子(CrO2-)。其平衡关系如下:
Cr3++3OH-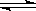 Cr(OH) 3
Cr(OH) 3 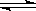 CrO2-+H++H2O
CrO2-+H++H2O
(紫色) (灰绿色) (亮绿色)
向0.05mol/L的Cr2(SO4) 3溶液50mL中,加入1.0mol/L的NaOH溶液50mL,充分反应后,溶液中可观察到的现象为
A.溶液为紫色 B.溶液为亮绿色
C.溶液中有灰绿色沉淀 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验的叙述中不正确的是( )
A.向某溶液中依次加入BaCl2溶液和稀盐酸,有不溶于稀盐酸的白色沉淀生成,则该溶液中一定含S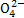
B.取醋酸钠溶液,用pH试纸检验,试纸变蓝,说明醋酸是弱酸
C.向装有碘水的分液漏斗中滴加CCl4,振荡、静置后分液,即可将碘萃取到CCl4中
D.读取滴定管内液体体积时,仰视读数,将导致读数偏大
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酰氯(SO2Cl2)是一种化工原料,有如下有关信息:
常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气。
氯化法是合成硫酰氯的常用方法,实验室合成反应和实验装置如下:
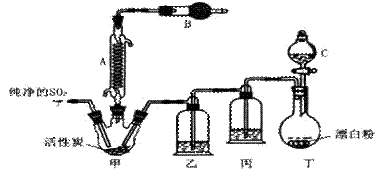
回答下列问题:
(1)仪器A的名称为______,甲中活性炭的作用是______,B中加入的药品是______。实验时从仪器C中放出溶液的操作方法是___________。
(2)装置丁中发生反应的离子方程式为___________。用亚硫酸钠固体和浓硫酸制备二氧化硫气体时,如要控制反应速度,下图中可选用的发生装置是________(填写字母)。
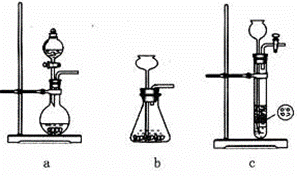
(3)氯磺酸(C1SO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为_________________,分离产物的方法是_________。
(4)若缺少装置乙,氯气和二氧化硫可能发生反应的化学方程式为_______。为提高本实验中硫酰氯的产率,在实验操作中还需要注意的事项有(只答一条即可)_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com