
����Ŀ�����ſ�ѧ�����ķ�չ�ͻ���Ҫ��IJ�����ߣ�CO2�IJ������ü�����Ϊ�о����ص㡣
���������գ�
��1��Ŀǰ���ʿռ�վ����CO2��һ����Ҫ�����ǽ�CO2��ԭ�����漰�ķ�Ӧ����ʽΪ��
CO2��g��+4H2��g��![]() CH4��g��+2H2O��g��
CH4��g��+2H2O��g��
��֪H2������������¶����߶����ӡ�
���¶ȴ�300������400�������´ﵽƽ�⣬�ж����б����и��������ı仯����ѡ����������������С��������������
v�� | v�� | ƽ�ⳣ��K | ת������ |
��2����ͬ�¶�ʱ��������Ӧ�ڲ�ͬ��ʼŨ���·ֱ�ﵽƽ�⣬�����ʵ�ƽ��Ũ�����±���
[CO2]/mol��L-1 | [H2]/mol��L-1 | [CH4]/mol��L-1 | [H2O]/mol��L-1 | |
ƽ���� | a | b | c | d |
ƽ���� | m | n | x | y |
a��b��c��d��m��n��x��y֮��Ĺ�ϵʽΪ_________��
��3��̼�H2CO3��Ki1=4.3��10-7��Ki2=5.6��10-11
���H2C2O4��Ki1=5.9��10-2��Ki2=6.4��10-5
0.1 mol/L Na2CO3��Һ��pH____________0.1 mol/L Na2C2O4��Һ��pH����ѡ��������������С����������������
��Ũ�ȵIJ�����Һ��̼����Һ�У�������Ũ�Ƚϴ����___________��
������Ũ�ȵIJ�����Һ��̼����Һ�������ϣ���Һ�и�������Ũ�ȴ�С��˳����ȷ����_____����ѡ���ţ�
a��[H+]��[HC2O4-]��[HCO3-]��[CO32-]
B��[HCO3-]��[HC2O4-]��[C2O42-]��[CO32-]
c��[H+]��[HC2O4-]��[C2O42-]��[CO32-]
D��[H2CO3] ��[HCO3-]��[HC2O4-]��[CO32-]
��4������ѪҺ�е�̼���̼�����δ���ƽ�⣺H++ HCO3-![]() H2CO3�������������Ի�������ʽ���ѪҺ��ʱ��ѪҺ��pH�仯������ƽ���ƶ�ԭ��������������
H2CO3�������������Ի�������ʽ���ѪҺ��ʱ��ѪҺ��pH�仯������ƽ���ƶ�ԭ��������������
____________________________________________________________________________________
���𰸡���1��
v�� | v�� | ƽ�ⳣ��K | ת������ |
���� | ���� | ��С | ��С |
��2��![]()
��3�����ڣ����ac
��4���������������ʽ���ѪҺ�У�ƽ�������ƶ���ʹH+Ũ�ȱ仯��С��ѪҺ��pH�������䣻�������������ʽ���ѪҺ�У�ƽ�������ƶ���ʹH+Ũ�ȱ仯��С��ѪҺ��pH�������䡣�����������֣�
��������
�����������1��H2������������¶ȵ����߶����ӣ���˵�������¶�ƽ�����淴Ӧ������У�������Ӧ�Ƿ��ȷ�Ӧ�������¶����淴Ӧ���ʾ�����ƽ�����淴Ӧ������У�ƽ�ⳣ����С����Ӧ���ת���ʼ�С��
��2����ͬ�¶�ʱƽ�ⳣ�����䣬��a��b��c��d��m��n��x��y֮��Ĺ�ϵʽΪ![]() ��
��
��3�����ݵ��볣����֪���������ǿ��̼�ᣬ��̼���Ƶ�ˮ��̶ȴ��ڲ����ƣ�����0.1 mol/L Na2CO3��Һ��pH����0.1 mol/L Na2C2O4��Һ��pH�����������ǿ��̼�ᣬ���Ũ�Ȳ�����Һ��̼����Һ�У�������Ũ�Ƚϴ���Dz��ᡣa��������������볣��������̼��ģ����Բ���������ĵ���̶Ⱦ�����̼��ģ������Һ��[H+]��[HC2O4-]��[C2O42-]��[HCO3-]��[CO32-]��a��ȷ��b������a�з�����֪b����c������a�з�����֪c��ȷ��d������a�з�����֪d����ѡac��
��4������ƽ���֪�������������ʽ���ѪҺ�У�ƽ�������ƶ���ʹH+Ũ�ȱ仯��С��ѪҺ�е�pH�������䣻�������������ʽ���ѪҺ�У�ƽ�������ƶ���ʹH+Ũ�ȱ仯��С��ѪҺ��pH�������䡣


 ������ȫ��������ϵ�д�
������ȫ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯�����ת��������ͼ��ʾ�����з�����������
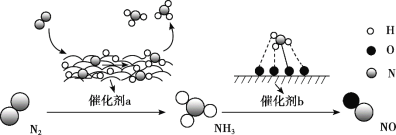
A. ����a���淢���˼��Թ��ۼ��Ķ��Ѻ��γ�
B. N2��H2��Ӧ����NH3��ԭ��������Ϊ100%
C. �ڴ���b�����γɵ�����ʱ�����漰����ת��
D. ����a��b����߷�Ӧ��ƽ��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2O2�ֽ������ܶ�������Ӱ�졣ʵ���� 70 ��ʱ��ͬ������H2O2Ũ����ʱ��ı仯��ͼ��ʾ������˵����ȷ����
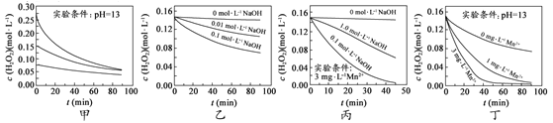
A.ͼ�ױ���������������ͬʱ��H2O2Ũ��ԽС����ֽ�����Խ��
B.ͼ�ұ���������������ͬʱ����ҺpHԽС��H2O2�ֽ�����Խ��
C.ͼ������������Mn 2+����ʱ����Һ����Խǿ��H2O2�ֽ�����Խ��
D.ͼ����ͼ��������������Һ�У�Mn2+��H2O2�ֽ����ʵ�Ӱ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʾ�й����ʼ����ʵ�������ȷ����( )
ѡ�� | ʵ����������� | ʵ����� |
A | ��ij��Һ�м��������ữ���Ȼ�����Һ���а�ɫ�������� | ����Һ��һ������ |
B | ��ij��Һ�м������ᣬ�����ɵ�����ͨ��Ʒ����Һ�У�Ʒ����Һ��ɫ | ����Һһ������ |
C | ��SO2ͨ��Na2CO3��Һ�����ɵ����壬��ͨ������������KMnO4��Һ����ͨ�����ʯ��ˮ���л��� | ˵�����ԣ�H2SO3��H2CO3 |
D | ��ij����ͨ��Ʒ����Һ�У�Ʒ����Һ��ɫ | ������һ����SO2 |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȫ��̬����������ܶȸߡ��ɱ��ͣ��乤��ԭ����ͼ��ʾ�����е缫 a���ò���ʯīϩ��S8���ϣ���ط�ӦΪ��16Li+xS8=8Li2Sx��2��x��8��������˵��������ǣ� ��
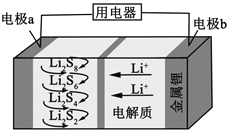
A. ��ع���ʱ�������ɷ�����Ӧ��2Li2S6+2Li++2e-=3Li2S4
B. ��ع���ʱ�����·������ 0.02 mol ���ӣ��������ϼ��� 0.14 g
C. ʯīϩ��������Ҫ����ߵ缫a�ĵ�����
D. ��س��ʱ��Խ���������Li2S2����Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ�������ʵ�ı�������ȷ����
A. ��Na��Cl�γ����Ӽ��Ĺ��̣�![]()
B. Na2S���������ɴ�����Hg2+�Ĺ�ҵ��ˮ��Hg2+��S2��=HgS��
C. CH3COOH��Һ��NaOH��Һ��Ӧ�ų�����H+(aq)��OH��(aq)=H2O(l) ��H����57.3 kJ��mol-1
D. ��п��ZnS����CuSO4��Һ����ת��Ϊͭ����CuS����ZnS��Cu2+=CuS��Zn2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W��Q��Ԫ�����ڱ��е����λ����ͼ��ʾ������˵����ȷ���ǣ� ��

A.�ǽ�����ǿ��˳��Ϊ��W>Q>Y
B.Ԫ��X��Ԫ��Z����������ϼ�֮�͵���ֵ����8
C.Z���ʺ�W������������Ӧ��ˮ����Ũ��Һ����Ӧ
D.�������ZQ3�����Ʊ�Z�ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡһ���������������������������Ʒ����ˮ�����100mL��Һ��������Һ�ֳɶ��ݣ��ڵ�һ����Һ�м���0.5mol��L-1�Ȼ���220mLǡ����ȫ��Ӧ���ڵڶ�����Һ��ͨ���״���µ�����0.896L����ʹFe2+ȫ�����Fe3+��
��1����ȡ��Ʒ�������������ʵ�����___��
��2���ڵ�һ����Һ��ȫ��Ӧ�����Һ���ټ�����������������Һ�����ó�����ϴ�Ӻ��ڿ����г�����գ��õ�������������___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ4A(s)+3B(g)![]() 2C(g)+D(g)��2min��B��Ũ�ȼ�����0.6mol��L-1������˵����ȷ���ǣ� ��
2C(g)+D(g)��2min��B��Ũ�ȼ�����0.6mol��L-1������˵����ȷ���ǣ� ��
A.��A��ʾ�Ļ�ѧ��Ӧ������0.4mol��L-1��min-1
B.�ֱ���B��C��D��ʾ��ѧ��Ӧ���ʣ������3��2��1
C.��2minĩ�ķ�Ӧ������B��ʾ��0.3mol��L-1��min-1
D.����2min��B��C�����ʵ�Ũ�ȶ���С
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com