
| A、能与Na2CO3反应生成CO2 |
| B、同浓度的HCl、CH3COOH稀溶液,CH3COOH的pH大 |
| C、CH3COONa溶液pH>7 |
| D、0.1mol/LCH3COOH溶液pH=1.5 |


 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
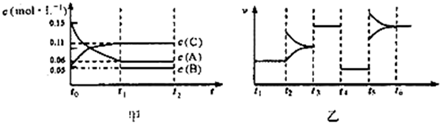
| A、其他条件不变时,增大压强,B的转化率不变 |
| B、t4~t5阶段改变的条件为降低温度 |
| C、B的起始物质的量为0.02mol |
| D、若t5~t6阶段改变的条件为升高温度,则正反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯酚有一定毒性,不能作消毒剂和防腐剂 |
| B、棉花、羊毛、木材主要成分都是纤维素 |
| C、油脂皂化生成的高级脂肪酸钠是肥皂的有效成分 |
| D、葡萄糖分子式为:CH2OH(CHOH)4CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它们的表面电镀上了一层耐磨的黄金 |
| B、环境污染日趋严重,它们表面的铜丝被酸雨溶解洗去 |
| C、铜的金属活动性比氢小,因此不易被氧化 |
| D、它们是含有一定比例的金、银、锡、锌的合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单质熔、沸点逐渐降低 |
| B、气态氢化物稳定性逐渐增强 |
| C、卤素离子的还原性逐渐增强 |
| D、单质的氧化性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Na+、OH-、Cl- |
| B、Ba2+、Cu2+、NO3-、SO42- |
| C、Mg2+、Na+、OH-、SO42- |
| D、H+、Ba2+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com