

如右图所示,把试管放入盛有25 ℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴加5 mL盐酸于试管中。试回答下列问题:
(1)实验中观察到的现象是______________________________。
(2)产生上述现象的原因是______________________________。
(3)写出有关反应的离子方程式:_______________________。
(4)由实验推知,镁片和盐酸的总能量________(填“大于”“小于”或“等于”)氯化镁溶液和氢气的总能量。
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Al、Mg | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Al、Mg | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
试根据上表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极(正极或负极)是否相同(填“是”或“否”)?________。
(2)对实验3完成下列填空:
①铝为________极,电极反应式:______________________。
②石墨为________极,电极反应式:_____________________。
③电池总反应式:_____________________________________。
(3)实验4中铝作负极还是正极________,理由是______________________________。写出铝电极的电极反应式:__________________________________________________。
(4)解释实验5中电流计指针偏向铝的原因:__________________________________________________。
(5)根据实验结果总结出影响铝在原电池中作正极或负极的因素:____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用A、B、C三种装置都可制取溴苯.请仔细分析三套装置,然后回答下列问题:
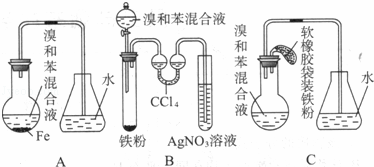
(1)写出三个装置中都发生反应的化学方程式:;
(2)装置A、C中长导管的作用是;
(3)B、C装置已连接好,并进行了气密性检验,也装入了合适的药品,接下来要使反应开始,对C应进行的操作是,反应过程中,B中盛放硝酸银试管中观察到的现象是生.
(4)A中存在加装药品和及时密封的矛盾,因而在实验中易造成的不良后果是.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H2(g)+F2(g)===2HF(g) ΔH=-270 kJ·mol-1,下列说法正确的是( )
A.2 L氟化氢气体分解成1 L氢气与1 L氟气吸收270 kJ热量
B.1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ
C.在相同条件下,1 mol氢气与1 mol氟气的能量总和大于2 mol氟化氢气体的能量
D.1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应N2+3H2===2NH3的能量变化如图所示,该反应的热化学方程式是( )
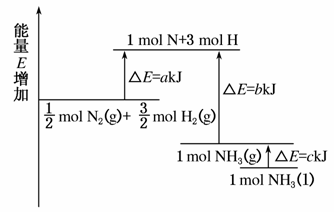
A.N2(g)+3H2(g)===2NH3(l)
ΔH=2(a-b-c)kJ·mol-1
B.N2(g)+3H2(g)===2NH3(g)
ΔH=2(b-a)kJ·mol-1
C. N2(g)+
N2(g)+ H2(g)===NH3(l)
H2(g)===NH3(l)
ΔH=(b+c-a)kJ·mol-1
D. N2(g)+
N2(g)+ H2(g)===NH3(g)
H2(g)===NH3(g)
ΔH=(a+b)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示为实验室中完成不同的化学实验所选用的装置或进行的操作,其中没有明显错误的是( )
| 测定中和热 | 用石灰石和稀盐酸制取 CO2 | 蒸馏石油 | 配制溶液中转移溶液 |
|
|
|
|
|
| A | B | C | D |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)氨气催化氧化生产硝酸,硝酸厂常用催化还原法处理尾气:催化剂存在时用H2将NO2还原为N2.已知:2H2(g)+O2(g)=2H2O(g)△H=﹣483.6kJ•mol﹣1 N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ•mol﹣1,则H2还原NO2生成水蒸气反应的热化学方程式是 .
(2)氮气和氢气合成氨是化学工业中极为重要的反应,其热化学方程式可表示为:N2(g)+3H2(g)⇌2NH3(g)△H=﹣92kJ•mol﹣1.请回答下列问题:
①取1mol N2(g)和3mol H2(g)放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量 92kJ(填“大于”“等于”或“小于”),原因是 .
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末考试化学试卷(解析版) 题型:选择题
下图甲和乙是双液原电池装置。由图可判断下列说法错误的是
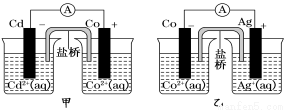
A.甲图电池反应的离子方程式为:Cd(s)+Co2+(aq)===Co(s)+Cd2+(aq)
B.2Ag(s)+Cd2+(aq)===Cd(s)+2Ag+(aq)反应能够发生
C.盐桥的作用是形成闭合回路,并使两边溶液保持电中性
D.乙图当有1 mol电子通过外电路时,正极有108 g Ag析出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com