
【题目】废旧金属可以回收利用,用合金废料(含铁、铜和铝)制取硫酸亚铁和硫酸铜溶液的实验流程如下(部分生成物已略):

(1)合金属于________(填“纯净物”或“混合物”)。
(2)步骤①反应的化学方程式为:2Al+2NaOH+2R=2NaAlO2+3H2↑,依据质量守恒定律推出R的化学式为_________。步骤②反应的化学方程式为_____________________________。
(3)由铜制取硫酸铜溶液有以下三种途径:
I.Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
II.2Cu+O2![]() 2CuO CuO+H2SO4=CuSO4+H2O
2CuO CuO+H2SO4=CuSO4+H2O
Ⅲ.3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
你认为最佳途径是____________(填序号),理由是___________________。
【答案】混合物 H2OFe+H2SO4=FeSO4+H2↑III会产生污染物二氧化硫,污染空气,并且硫酸的利用率低,III不产生硫酸铜,还产生污染物一氧化氮
【解析】
(1)合金是金属和金属,金属和非金属经过熔合得到的,混合物是由两种或多种物质组成的,所以合金属于混合物;
(2)生成物中有2个钠原子,2个铝原子,4个氧原子,6个氢原子,反应物中有2个铝原子,2个钠原子、氢原子、氧原子,所以R是H2O;铁和稀硫酸反应生成硫酸亚铁和氢气,化学方程式为Fe+H2SO4=FeSO4+H2↑;
(3)由于I会产生污染物二氧化硫,污染空气,并且硫酸的利用率低,III不产生硫酸铜,还产生污染物一氧化氮,所以最佳途径是Ⅱ。


科目:高中化学 来源: 题型:
【题目】下列关于有机物的描述你认为正确的是:
A.含碳元素的化合物一定是有机化合物
B.乙烷和乙烯互为同系物
C.苯分子含有碳碳双键,所以可以使酸性高锰酸钾褪色
D.正丁烷和异丁烷互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为五种气态烃,其中A、B、C都能使酸性高锰酸钾溶液褪色;1mol C能与2mol Br2完全加成,生成物分子中每个碳原子上有一个溴原子;A与C具有相同的通式;A与H2加成可得B,B与相同条件下N2的密度相同;D是最简单的有机物,E是D的同系物,完全燃烧相同物质的量的B或E生成CO2的量相同。
(1)试确定A、B、C、D、E的结构简式:
A:_____;B:_____;C:_____;D:_____;E:_____。
(2)等质量的A、B、C、D、E完全燃烧,耗氧量最多的是______(填名称,下同)生成二氧化碳最多的是______。
(3)等物质的量的A、B、C、D、E完全燃烧,耗氧量最多的是____(填名称,下同),生成水最多的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取盐酸与氯化铜的混合溶液27g放入烧杯中,逐滴滴入质量分数为20%的氢氧化钠溶液,产生沉淀质量与滴入氢氧化钠溶液质量关系如图所示。
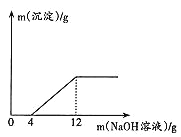
(1)滴入氢氧化钠溶液的质量在0~4g时,发生反应的化学方程式为___________。
(2)与氯化铜反应的氢氧化钠的质量为____________g。
(3)求原盐酸与氯化铜的混合溶液中氯化铜的质量分数______(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 136g熔融的KHSO4中含有2NA个阳离子
B. 40gH218O与40gD2O所含的中子数均为20NA
C. 1molFe分别与足量的稀硫酸和稀硝酸反应转移电子数均为2NA
D. 标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~E是初中化学常见的物质:盐酸、氢氧化钠、氢氧化钙、碳酸钠、二氧化碳中的某一种。A可用于金属表面除锈,B可用来改良酸性土壤。它们相互之间发生反应或转化的关系如右图所示(“-”表示两种物质间能发生反应,“→”表示两种物质间的转化关系)。

(1)A、C的化学式分别为________、________;D在生活和生成中的一种用途是_________。
(2)E→D反应的化学方程式为_____________________________;B与D反应的化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(能力挑战题)已知五种元素的原子序数的大小顺序为C>A>B>D>E;A、C同周期,B、C同主族;A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30,D和E可形成4核10个电子分子。试回答下列问题:
(1)写出五种元素的名称。
A ,B ,C ,D ,E 。
(2)用电子式表示离子化合物A2B的形成过程:_________ ____________。
(3)写出D元素形成的单质的结构式: ____________________。
(4)写出下列物质的电子式:
E与B形成的化合物: ;A、B、E形成的化合物: ;D、E形成的化合物: ___________。
(5)A、B两元素组成的化合物A2B2属于 (填“离子”或“共价”)化合物,存在的化学键是 ,写出A2B2与水反应的化学方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.水和冰互为同素异形体B.35Cl和37Cl互为同位素
C.白磷与红磷互为同位素D.CH4和CH3CH3互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿文同学想测定某Cu-Ag合金中两种金属的质量比。称取这种合金9.6g,加入足量AgNO3溶液充分反应后过滤,将所得固体洗涤、干燥后称量,质量为24.8g。
(1)发生反应的化学方程式为______________________。
(2)试计算该合金中铜与银的质量比__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com