
分析 还原性大小为:I->Br-,通入氯气后I-优先反应,I-反应完全后Br-开始反应;0.1molNaBr完全反应消耗0.05mol氯气,0.2molNaI完全反应消耗0.1mol氯气,
当氯气过量时,消耗氯气的总体积为:22.4L/mol×(0.05mol+0.1mol)=3.36L;当碘离子恰好完全反应时,0.2molNaI完全反应消耗氯气的物质的量为0.1mol,标准状况下的体积为2.24L;当碘离子完全反应、溴离子部分反应时,则2.24L≤v<3.36L,据此进行解答.
解答 解:还原性大小为:I->Br-,通入氯气后I-优先反应,I-反应完全后Br-开始反应,
0.1molNaBr完全反应消耗0.05mol氯气,0.2molNaI完全反应消耗0.1mol氯气,
当氯气过量时,消耗氯气的总体积为:22.4L/mol×(0.05mol+0.1mol)=3.36L,
v的取值范围为0<v<2.24L时,氯气的物质的量为小于0.1mol,此时碘离子有剩余,NaBr没有反应,则固体剩余物质成分是:NaBr、NaI、NaCl;
当固体剩余物质成分是NaCl时,说明氯气足量,则氯气的体积v的范围为:v≥3.36L;
当固体剩余物质成分是NaCl和NaBr时,说明碘离子完全反应、溴离子部分反应,则氯气的体积v的范围为:2.24L≤v<3.36L,
故答案为:NaBr、NaI、NaCl;v≥3.36L;2.24L≤v<3.36L.
点评 本题考查了有关范围讨论的计算,题目难度中等,明确发生反应的实质及先后顺序为解答关键,注意掌握讨论法在化学计算中的应用方法,试题充分考查学生的分析、理解能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
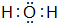 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯是由乙烯加聚生成的纯净物 | |
| B. | 蛋白质和淀粉水解的最终产物都是氨基酸 | |
| C. | 油脂、纤维素、淀粉在一定条件下均可发生水解反应 | |
| D. | 蛋白质、纤维素、蔗糖都是高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.8g C2H4和C3H6的混合物中含碳原子数为0.2×6.02×1023 | |
| B. | 在O2参与的反应中,1 mol O2做氧化剂时,得到电子数一定是4×6.02×1023 | |
| C. | 1 L 0.1 mol/L 的Na2S溶液中硫离子数为0.1×6.02×1023 | |
| D. | 标准状况下,11.2 L乙醇中氧原子数为0.5×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
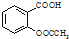 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
| 名称 | 相对分子质量 | 熔点或沸点 (℃) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 反应 |
| 乙烯水杨酸 | 180 | 135(熔点) | 微溶 |


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com