
下列有关化学研究的正确说法是( )
|
| A. | 同时改变两个变量来研究反映速率的变化,能更快得出有关规律 |
|
| B. | 对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同 |
|
| C. | 依据丁达尔现象可将分散系分为溶液、胶体与浊液 |
|
| D. | 从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属递增的规律 |
考点:
用盖斯定律进行有关反应热的计算;分散系、胶体与溶液的概念及关系;化学反应速率的影响因素;卤素原子结构及其性质的比较.
专题:
化学反应中的能量变化;化学反应速率专题.
分析:
A.同时改变两个变量来研究反应速率的变化,不容易判断影响反应速率的主导因素,因此更难得出有关规律;
B.这是盖斯定律的表述;
C.分散系的划分是以分散质颗粒大小来区分的;
D.在以酸性强弱作为判断元素非金属性强弱时,是以最高价氧化物对应水化物的酸性强弱为判断依据的.
解答:
解:A.同时改变两个变量来研究反应速率的变化,不容易判断影响反应速率的主导因素,因此更难得出有关规律,应改变一个变量,故A错误;
B.根据盖斯定律可知,对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同,故B正确;
C.分散系的划分是以分散质颗粒大小来区分的,胶体粒子直径介于1nm~100nm之间,溶液溶质粒子直径小于1nm,浊液粒子直径大于100nm,溶液和浊液都不具有丁达尔效应,故C错误;
D.元素非金属性强越强,对应的最高价氧化物对应水化物的酸性越强,与氢化物的酸性无关,故D错误.
故选B.
点评:
本题侧重考查反应速率、盖斯定律、分散系、元素周期律重要的基本概念、规律,题目难度不大.


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化.某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式如下:
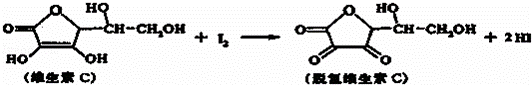
下列说法正确的是( )
|
| A. | 维生素C的分子式为C6H8O6 |
|
| B. | 维生素C在酸性条件下水解得到3种产物 |
|
| C. | 维生素C不溶于水,可溶于有机溶剂 |
|
| D. | 上述反应为取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
金属镍及其化合物在合金材料以及催化剂等方面应用广泛。根据要求回答下列问题:
(1)基态Ni的价电子构型(电子排布式)为______________________。
(2)Ni(CO)4常温为液态,易溶于CCl4、苯等有机溶剂,则Ni(CO)4属于_______晶体。
(3)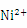 可与丁二酮肟(
可与丁二酮肟(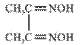 )作用生成腥红色配合物沉淀A。
)作用生成腥红色配合物沉淀A。
①丁二酮肟分子中碳原子的杂化轨道类型有______________,1mol该分子中含有的碳碳σ键和碳氮σ键的总数为__________。
②氨气在水中的溶解度远大于甲烷,其原因是____________。
③腥红色配合物沉淀A中(结构如下)除含有一般共价键外,还含有配位键和氢键,请在下图中标出配位键和氢键。
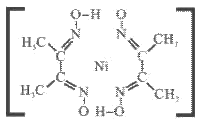
(提示: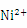 的配位数为4,配位键用“→”表示,氢键用“…”表示)
的配位数为4,配位键用“→”表示,氢键用“…”表示)
(4)据报道,某种含有镁、镍和碳三种元素的晶体具有超导性,该新型超导晶体的一个晶胞的结构如下图所示,则该晶体的化学式为__________。
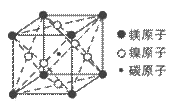
查看答案和解析>>
科目:高中化学 来源: 题型:
)下列溶液中微粒的物质的量浓度关系正确的是( )
|
| A. | Ca(ClO)2溶液中:c(Ca2+)>c(ClO﹣)>c(OH﹣)>c(H+) |
|
| B. | 等体积、等物质的量浓度的NaX和弱酸HX混合:c(Na+)=c(X﹣)>c(OH﹣)=c(H+) |
|
| C. | 常温下,将25mL0.2mol/L的盐酸与100mL0.1mol/L的氨水混合,所得溶液中:c(NH4+)>c(Cl﹣)>c(NH3•H2O)>c(OH﹣)>c(H+) |
|
| D. | 将0.1mol/L的Na2S溶液与0.1mol/L的NaHS溶液等体积混合,所得溶液中:c(S2﹣)+2c(OH﹣)=2c(H+)+c(HS﹣)+3c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是
(用必要的化学用语和相关文字说明).
(2)相同条件下,0.1mol•L﹣1 NH4Al(SO4)2中c(NH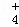 ) (填“等于”“大于”或“小于”)0.1mol•L﹣1 NH4HSO4中c(NH
) (填“等于”“大于”或“小于”)0.1mol•L﹣1 NH4HSO4中c(NH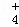 ).
).
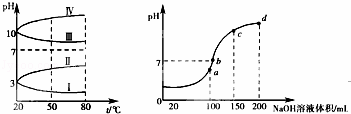
(3)如图1所示是0.1mol•L﹣1电解质溶液的pH随温度变化的图象.
①其中符合0.1mol•L﹣1 NH4Al(SO4)2的pH随温度变化的曲线是 (填写序号),导致pH随温度变化的原因是 ;
②20℃时,0.1mol•L﹣1 NH4Al(SO4)2中2c(SO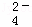 )﹣c(NH
)﹣c(NH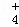 )﹣3c(Al3+)= (填数值).
)﹣3c(Al3+)= (填数值).
(4)室温时,向100mL 0.1mol•L﹣1 NH4HSO4溶液中滴加0.1mol•L﹣1 NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图2所示:试分析图中a、b、c、d四个点,水的电离程度最大是 点;在b点,溶液中各离子浓度由大到小的排列顺序是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既属于氧化还原反应,又属于吸热反应的是( )
|
| A. | 铝片和稀盐酸反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 |
|
| C. | 甲烷在氧气中的燃烧反应 | D. | 灼热的碳与二氧化碳的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,往容积恒定的密闭容器中投入2molA和1molB,发生可逆反应:2A(g)+B(g)⇌C(g)+D(s),达到平衡时,测得压强为原压强的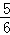 ,则A的转化率为( )
,则A的转化率为( )
|
| A. | 25% | B. | 40% | C. | 50% | D. | 75% |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中错误的是( )
A. 质量相等,密度不等的N2和C2H4两种气体含有的分子数一定相等
B. 同温同压下,等体积的H2和He气含有的质子数相等
C. 某物质经分析仅含一种元素,此物质可能是纯净物也可能是混合物
D. FeCl3溶液呈电中性,Fe(OH)3胶体带有电荷
查看答案和解析>>
科目:高中化学 来源: 题型:
如图图表示各物质之间的转化关系.
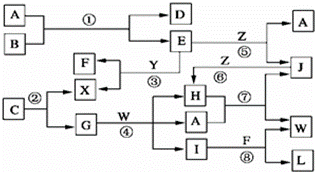
已知:
(1)A是无色液体,L是不溶于稀硝酸的白色沉淀,E、F、H、J、X、Y和Z都是气体;
(2)G、X、Y和Z都是单质,其它是化合物,其中Y呈黄绿色,H呈红棕色,E和F都极易溶解于水,二者相遇会有白烟生成.
(3)B和C都是由一种金属与一种非金属元素组成的化合物,其中非金属元素相同且价态也相同,B中非金属元素的质量分数为28%,组成B的金属元素原子核外的K层和M层电子数相同.
请根据以上信息完成下列要求:
(1)写出下列物质的化学式:C ,F ,H
(2)写出E的电子式
(3)实验室制Y的离子方程式为
(4)上述反应中是氧化还原反应的除了②、③、④和⑦外,还有(填反应代号)
(5)写出反应①④⑤的化学反应方程式
①
④
⑤
(6)保持容器的温度和体积不变,在反应③刚好完全反应时,反应前后容器的压强之比为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com