

分析 (1)LiaMnbOc中锂显+1价,氧显-2价,设Mn的化合价为+x,根据化合价代数和为零求锰的化合价
(2)用高锰酸钾溶液滴定剩余的草酸钠,当滴定完全后,显示高锰酸钾的颜色,当滴入最后一定高锰酸钾溶液,溶液由无色变为浅红色,且30s内不褪色;高锰酸钾在酸性条件下,发生自身氧化还原反应,生成二氧化锰及氧气;
(3)n(Na2C2O4)=0.2000mol/L×0.01L=2.000×10-3mol,
n(KMnO4)=0.02000mol/L×0.022L=4.400×10-4mol,
还原Mn4+、Mn3+的草酸钠为2.000×10-3mol-$\frac{5}{2}$×4.400×10-4mol=9.000×10-4mol,
n(Mn4+)+$\frac{1}{2}$n(Mn3+)=9.000×10-4mol ①
锰酸锂(LiaMnbOc)中总锰量为n(Mn4+)+n(Mn3+)+n(Mn2+)=n[(NH4)2Fe(SO4)2]-n(KMnO4)=0.1000mol/L×0.0164L-4.400×10-4mol=1.2000×10-3mol②,最后锰根据锰的总化合价除以锰的总物质的量为平均价态.
解答 解:(1)LiaMnbOc中锂显+1价,氧显-2价,设Mn的化合价为+x,根据化合价代数和为零,a+bx-2c=0,x=+$\frac{2c-a}{b}$;
故答案为:+$\frac{2c-a}{b}$;
(2)用高锰酸钾溶液滴定剩余的草酸钠,当滴定完全后,显示高锰酸钾的颜色,当滴入最后一定高锰酸钾溶液,溶液由无色变为浅红色,且30s内不褪色;高锰酸钾在酸性条件下,发生自身氧化还原反应,生成二氧化锰及氧气,离子方程式为4MnO4-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$4MnO2+2H2O+3O2↑;
故答案为:当滴入最后一定高锰酸钾溶液,溶液由无色变为浅红色,且30s内不褪色;4MnO4-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$4MnO2+2H2O+3O2↑;
(3)n(Na2C2O4)=0.2000mol/L×0.01L=2.000×10-3mol,
n(KMnO4)=0.02000mol/L×0.022L=4.400×10-4mol,
还原Mn4+、Mn3+的草酸钠为2.000×10-3mol-$\frac{5}{2}$×4.400×10-4mol=9.000×10-4mol,
n(Mn4+)+$\frac{1}{2}$n(Mn3+)=9.000×10-4mol ①
锰酸锂(LiaMnbOc)中总锰量为n(Mn4+)+n(Mn3+)+n(Mn2+)=n[(NH4)2Fe(SO4)2]-n(KMnO4)=0.1000mol/L×0.0164L-4.400×10-4mol=1.2000×10-3mol ②,锰酸锂样品中锰的平均价态为$\frac{4n(M{n}^{4+})+3n(M{n}^{3+})+2n(M{n}^{2+})}{n(M{n}^{4+})+n(M{n}^{3+})+n(M{n}^{2+})}$=$\frac{2(①+②)}{②}$=$\frac{4.2000×1{0}^{-3}mol}{1.2000×1{0}^{-3}mol}$=+3.50,
故答案为:+3.50.
点评 本题考查连续滴定法测定锰酸锂(LiaMnbOc)中锰元素的平均价态,难度较大,注意锰的总化合价除以锰的总物质的量为平均价态.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥⑦⑧ | B. | ①④⑤⑥⑦ | C. | ④⑤⑥⑦⑧ | D. | ③④⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
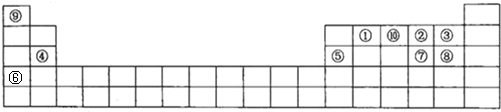
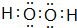 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 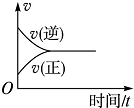 | B. | 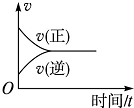 | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH=CH3COO-+H+ | B. | NaOH=Na++OH- | ||
| C. | NH4Cl?NH4++Cl- | D. | NaHCO3=Na++H++CO32-. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用药匙取用粉末状或颗粒状固体 | B. | 用胶头滴管滴加少量液体 | ||
| C. | 倾倒液体时试剂瓶标签面向手心 | D. | 给盛有$\frac{2}{3}$体积液体的试管加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com