
某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
A.该温度高于25℃
B.由水电离出的[H+]=1.0×10-10 mol·L-1
C.加入NaHSO4晶体抑制了水的电离
D.该温度下加入等体积pH=12的NaOH溶液可使该溶液恰好呈中性
科目:高中化学 来源: 题型:
下表是A、B两种有机物的有关信息:
| A | B |
| ①能使溴的四氯化碳溶液褪色; ②比例模型为 ③能与水在一定条件下反应 | ①由C、H两种元素组成; ②球棍模型为: |
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称叫做
________________________________________________________________________;
写出在一定条件下,A生成高分子化合物的化学反应方程式:
________________________________________________________________________。
(2)A与氢气发生加成反应后生成C,与C在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2。当n=________时,这类有机物开始出现同分异构体。
(3)B具有的性质是________(填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤能使酸性KMnO4溶液和溴水褪色、⑥任何条件下不与氢气反应。
写出在浓硫酸作用下,B与浓硝酸在60℃反应的化学方程式:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
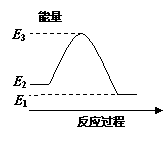
.反应X(g)+Y(g)  2Z(g) ΔH<0,达到平衡时,下列说法正确的是
2Z(g) ΔH<0,达到平衡时,下列说法正确的是
A.减小容器体积,平衡向右移动 B.加入催化剂,Z的产率增大
C.增大c(X),X的转化率增大 D.降低温度,Y的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
.下列有关说法正确的是( )
A.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0
B.高温下,工业上用纯碱和石英砂制玻璃,说明硅酸的酸性强于碳酸
C.加热蒸干氯化铝溶液并灼烧残留物至质量不变,所得固体为氧化铝
D.高温下,用金属钠与氯化钾可以置换出金属钾,说明钠的金属性比钾强
查看答案和解析>>
科目:高中化学 来源: 题型:
水是最宝贵的资源之一。下列表述正确的是( )
A.H2O的电子式为H+[
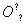
 H]-
H]-
B.4℃时,纯水的pH=7
C.D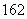 O中,质量数之和是质子数之和的两倍
O中,质量数之和是质子数之和的两倍
D.273 K、101 kPa,水分子间的平均距离d:d(气态)>d(液态)>d(固态)
查看答案和解析>>
科目:高中化学 来源: 题型:
有一学生在实验室测某溶液的pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作是__________(填“正确”或“错误”)的,其理由是
________________________________________________________________________。
(2)如不正确,请分析是否一定有误差
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)若用此法分别测定[H+]相等的盐酸和醋酸溶液的pH,误差较大的是__________,原因是________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将蔗糖溶于水配成10%的溶液,分装在两个试管中。在第一个试管中加入几滴稀硫酸并水浴加热,然后再加入新制的Cu(OH)2悬浊液并加热,没有砖红色沉淀产生,原因是______________________________;在第二个试管中加入几滴稀硫酸,再放在水浴中加热,再加入足量的NaOH溶液并加入新制的Cu(OH)2悬浊液,加热后的现象是________________,加入足量NaOH溶液的作用是______________________________。上述实验中发生反应的化学方程式是___________________________________
_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
核黄素又称维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳。核黄素分子的结构为:
已知: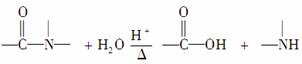 有关核黄素的下列说法中,不正确的是( )
有关核黄素的下列说法中,不正确的是( )
A.该化合物的分子式为C17H22N4O6
B.酸性条件下加热水解,有CO2生成
C.酸性条件下加热水解,所得溶液加碱后有NH3生成
D.能发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D是四种短周期元素,E是过渡元素,A、B、C同周期,C、D同主族,A的原子结构示意图为: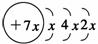 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)写出下列元素的符号:A________,B________,C________,D________。
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是________,碱性最强的是________。
(3)用元素符号表示D所在周期第一电离能最大的元素是________,电负性最大的元素是________。
(4)画出D的核外电子排布图________,这样排布遵循了________原理和________规则。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com