
| A��HCl��NaOH��Ӧ���м��ȡ�H ="-57.3" kJ/mol����H2SO4��Ca(OH) 2��Ӧ�� �к��ȡ�H =2����-57.3��kJ/mol |
B��CO��g����ȼ������283.0 kJ/mol����2CO2��g�� 2CO��g��+O2��g����Ӧ 2CO��g��+O2��g����Ӧ�ġ�H =" +2��283.0" kJ/mol |
| C����Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ |
| D��1 mol����ȼ��������̬ˮ�Ͷ�����̼���ų��������Ǽ����ȼ���� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NF3 | B��CH3�� | C��BF3 | D��H3O+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2HI��g��+9��48kJ
2HI��g��+9��48kJ 2HI��g��-26��48kJ
2HI��g��-26��48kJ| A�����е�I2Ϊ��̬�����е�I2Ϊ��̬ |
| B���ڵķ�Ӧ���������Ȣٵķ�Ӧ���������� |
| C���ٵIJ���ȷ�Ӧ�ڵIJ������ȶ��Ը��� |
| D��1mol ��̬������ʱ������17kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2HI(g) ��H=��a kJ��mol��1
2HI(g) ��H=��a kJ��mol��1 ��a��b��c�������㣩
��a��b��c�������㣩| A����Ӧ�������������������������� |
| B���Ͽ�1 mol H-H����1 mol I-I�������������ڶϿ�2 mol H-I���������� |
| C���Ͽ�2 mol H-I����������ԼΪ(c+b+a) kJ |
| D�����ܱ������м���2 mol H2��2 mol I2����ַ�Ӧ��ų�������С��2a kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��1 molʯī���ܼ��ܱ�1 mol���ʯ���ܼ���С1.9 kJ |
| B��ʯī�ͽ��ʯ��ת���������仯 |
| C�����ʯ���ȶ���ǿ��ʯī |
| D��C��s��ʯī��==C��s�����ʯ�� ��H=" +1.9" kJ?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����֪CH4(g)��2O2(g)=CO2(g)��2H2O(g) ��H��-802 kJ/mol�������ȼ����Ϊ802 kJ/mol |
| B������H2��O2����ȫȼ�գ�����H2O(g)������H2O(l)�ų��������� |
| C��ͬ��ͬѹ�£�H2(g)��Cl2(g)=2HCl(g)�ڹ��պ͵�ȼ�����µĦ�H��ͬ |
| D����ʯī�Ƚ��ʯ�ȶ���֪��C(���ʯ, s)=C(ʯī, s) ��H<0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
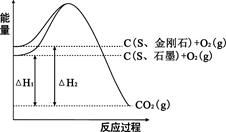
| A�����ʯ��ʯī�ȶ� |
| B��C��s��ʯī����C��s�����ʯ����H ����1��5kJ/mol |
| C����H1����H2 |
| D�����ʹ�ô�������H1�͡�H2����С |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com