
| A. | 原子的核外电子排布呈周期性变化 | B. | 原子半径呈周期性变化 | ||
| C. | 原子的电子层数呈周期性变化 | D. | 化合价呈周期性变化 |
分析 随原子序数的递增,原子的结构呈现周期性的变化而引起元素的性质的周期性变化,以此来解答.
解答 解:A.因原子的核外电子排布中电子层数和最外层电子数都随原子序数的递增而呈现周期性变化,则引起元素的性质的周期性变化,故A正确;
B.因元素的原子半径是元素的性质,不能解释元素性质的周期性变化,故B错误;
C.由原子的电子排布可知,随原子序数的递增,电子层数呈现周期性的变化,与元素性质的周期性变化有关,但不是唯一因素,而是电子层数和最外层电子数都呈现周期性的变化而引起元素性质的周期性变化,即原子的电子层排布的周期性变化是引起元素性质周期性变化的决定因素,故C错误;
D.因元素的化合价属于元素的性质,则不能解释元素性质的周期性变化,故D错误;
故选A.
点评 本题考查元素周期律的实质,为高频考点,明确原子的结构与性质的关系、元素的性质有哪些是解答的关键,并注意不能用元素本身的性质来解释元素性质的周期性变化,题目难度不大.


科目:高中化学 来源: 题型:解答题

 .
. +NaHCO3→
+NaHCO3→ +H2O+CO2↑.
+H2O+CO2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯、苯、乙醇均能使紫色的酸性高锰酸钾溶液褪色 | |
| B. | 用新制的银氨溶液可区分甲酸乙酯和乙醛 | |
| C. | 油脂在碱的作用下可发生水解,工业上利用该反应生产肥皂 | |
| D. | 乙酸乙酯、油脂、果糖、蛋白质都可以发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  实验室制乙烯 | |
| B. | 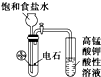 实验室制乙炔并验证乙炔发生氧化反应 | |
| C. | 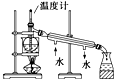 实验室中分馏石油 | |
| D. | 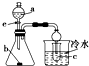 若a为醋酸,b为贝壳(粉状),c为苯酚钠溶液,验证醋酸、碳酸、苯酚酸性的强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 +H2O(未配平),下列有关说法正确的是( )
+H2O(未配平),下列有关说法正确的是( )| A. | 该反应属于中和反应 | B. | 三聚氰胺的分子式为C3H6N3O3 | ||
| C. | 三聚氰胺分子中只有极性键 | D. | 三聚氰胺属于离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 此滴定实验可以选用酚酞做指示剂 | B. | 在A点:c(Cl-)>c(H+)>c(NH4+)>c(OH-) | ||
| C. | 在B点:c(H+)=c(OH-)=c(Cl-)=c(NH4+) | D. | 在C点:c(NH4+)+c(NH3•H2O)=2c(Cl-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com