
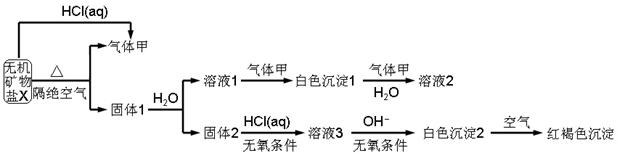



 ŠÄĖćæŚĖćĒÉĖćŅ»æĪŅ»Į·ĻµĮŠ“š°ø
ŠÄĖćæŚĖćĒÉĖćŅ»æĪŅ»Į·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ļ”ĮņĖį | B£®ĮņĖįŃĒĢśČÜŅŗ |
| C£®ĮņĖįĶČÜŅŗ | D£®Ź³ŃĪĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ÖĘ·¹É×”¢·¹ŗŠ”¢øßŃ¹¹ųµČµÄ²»ŠāøÖŹĒŗĻ½š |
| B£®×öŅĀ·žµÄĆŽŗĶĀé¾łÓėµķ·Ū»„ĪŖĶ¬·ÖŅģ¹¹Ģå |
| C£®¼åÕØŹ³ĪļµÄ»ØÉśÓĶŗĶÅ£ÓĶ¶¼ŹĒæÉŌķ»ÆµÄ±„ŗĶõ„Ąą |
| D£®Ä„¶¹½¬µÄ“ó¶¹ø»ŗ¬µ°°×ÖŹ£¬¶¹½¬Öó·Šŗóµ°°×ÖŹ±ä³ÉĮĖ°±»łĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā
| ³ĮµķĪļ | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| æŖŹ¼³Įµķ | 1.3 | 3.3 | 7.5 | 10.3 |
| ĶźČ«³Įµķ | 2.8 | 5.2 | 9.7 | 12.2 |
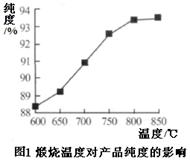
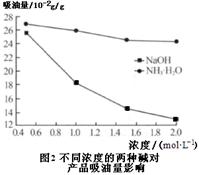
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
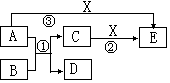
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
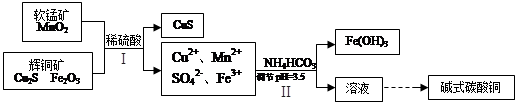
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā
|
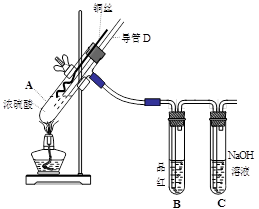
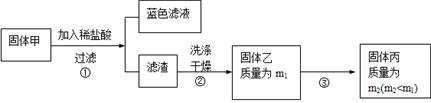 £Ø3£© ¹ĢĢåŅŅŌŚæÕĘųÖŠģŃÉÕŹ±£¬Ź¹ÓƵďµŃéŅĒĘ÷³żĮĖ²£Į§°ō”¢Čż½Å¼Ü”¢¾Ę¾«µĘĶā£¬»¹±ŲŠėÓŠ£ŗ ”£
£Ø3£© ¹ĢĢåŅŅŌŚæÕĘųÖŠģŃÉÕŹ±£¬Ź¹ÓƵďµŃéŅĒĘ÷³żĮĖ²£Į§°ō”¢Čż½Å¼Ü”¢¾Ę¾«µĘĶā£¬»¹±ŲŠėÓŠ£ŗ ”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĄūÓĆĢś¼ÓČėĮņĖįĶČÜŅŗÖŠµÄ·“Ó¦æÉŅŌ±Č½ĻCu”¢Fe2+µÄ»¹ŌŠŌ |
| B£®×ćĮæµÄĶøśŅ»¶ØĮæµÄÅØĻõĖį·“Ó¦Ö»²śÉśŅ»ÖÖĘųĢå |
| C£®µŖµÄ¹Ģ¶ØÖ»ÓŠŌŚøßĪĀ”¢øßŃ¹”¢“߻ƼĮµÄĢõ¼žĻĀ²ÅÄÜŹµĻÖ |
| D£®ŅŌĢśĪŖŅõ¼«”¢ĶʬĪŖŃō¼«”¢ĮņĖįĶĪŖµē¶ĘŅŗæÉŅŌŹµĻÖĢśÖĘĘ·¶ĘĶ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com