
【题目】下列说法正确的是( )
A.在接触室里用98.3%的浓硫酸吸收SO3 , 目的是防止形成酸雾便于SO3吸收完全
B.工业制玻璃和炼铁过程中都要加入石灰石,目的是除去杂质二氧化硅
C.工业上用金属钠与TiCl4溶液在高温下反应,目的是将金属钛从氯化物中置换出来
D.海水中提取镁的过程中加入贝壳煅烧制得的石灰,目的是将Mg2+转变成Mg(OH)2
【答案】AD
【解析】解:A.在吸收塔中三氧化硫与水反应生成硫酸,但水直接吸收三氧化硫会形成酸雾,使三氧化硫的吸收率降低,生产实践中用98.3%的浓H2SO4吸收三氧化硫,可以防止形成酸雾,使SO3吸收完全,故A正确;
B.炼铁材料为铁矿石、焦炭、石灰石,加入石灰石,目的是除去杂质二氧化硅,普通玻璃的原料有砂子,石灰石和纯碱,石灰石是制玻璃的原料之一,故B错误;
C.工业上生产钛是在高温下用熔融TiCl4与钠反应制得,钠与TiCl4溶液在高温下不能置换出钛,故C错误;
D.把贝壳制成石灰乳[Ca(OH)2],发生的反应为CaCO3 ![]() CaO+CO2↑、CaO+H2O=Ca(OH)2,在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物,发生的反应为Mg2++2OH﹣=Mg(OH)2↓,所以加入贝壳煅烧制得的石灰,目的是将Mg2+转变成Mg(OH)2,故D正确;
CaO+CO2↑、CaO+H2O=Ca(OH)2,在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物,发生的反应为Mg2++2OH﹣=Mg(OH)2↓,所以加入贝壳煅烧制得的石灰,目的是将Mg2+转变成Mg(OH)2,故D正确;
故选AD.


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】若用AG表示溶液的酸度(acidity grade),AG的定义为AG=lg[ ![]() ].室温下实验室中用0.01molL﹣1的氢氧化钠溶液滴定20.00mL0.01molL﹣1的醋酸,滴定过程如图所示,下列叙述正确的是( )
].室温下实验室中用0.01molL﹣1的氢氧化钠溶液滴定20.00mL0.01molL﹣1的醋酸,滴定过程如图所示,下列叙述正确的是( ) 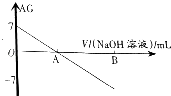
A.室温下,醋酸的电离常数约为10﹣5
B.A点时加入氢氧化钠溶液的体积为20.00mL
C.若B点为40mL,所得溶液中:c(H+)=c(CH3COO﹣)+c(CH3COOH)
D.反应过程中一定存在:0.01molL﹣1+c(OH﹣)=c(Na+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气排放的一氧化碳、氮氧化物等气体已成为大气污染的主要来源.德国大众汽车尾气检测造假事件引起全世界震惊.根据下列示意图回答有关问题: 
(1)汽车发动机工作时会引发N2(g)+O2(g)=2NO(g)△H=+180kJmol﹣1 , 其能量变化示意图如下: ![]()
则NO中氮氧键的键能为kJmol﹣1;
(2)空燃比过小易产生CO.有人提出可以设计反应2CO(g)=2C(s)+O2(g)来消除CO的污染.判断该设想是否可行,并说出理由;
(3)利用活性炭涂层排气管处理NOx的反应为:xC(s)+2NOx(g)N2(g)+xCO2 (g)△H=﹣b kJmol﹣1 . 若使NOx更加有效的转化为无毒尾气排放,以下措施理论上可行的是;
A.增加排气管长度
B.增大尾气排放口
C.升高排气管温度
D.添加合适的催化剂
(4)催化装置中涉及的反应之一为:2NO(g)+2CO(g)N2(g)+2CO2(g). 
①探究上述反应中NO的平衡转化率与压强、温度的关系,得到图2所示的曲线.催化装置比较适合的温度和压强是;
②测试某型号汽车在冷启动(冷启动指发动机水温低的情况下启动)时催化装置内CO和NO百分含量随时间变化曲线如图3所示.则前10s 内,CO和NO百分含量没明显变化的原因是;
③研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了以下三组实验:
实验编号 | T(K) | NO初始浓度 | CO初始浓度 | 催化剂的比表面积(m2/g) |
Ⅰ | 400 | 1.00×10﹣3 | 3.60×10﹣3 | 82 |
Ⅱ | 400 | 1.00×10﹣3 | 3.60×10﹣3 | 124 |
Ⅲ | 450 | 1.00×10﹣3 | 3.60×10﹣3 | 124 |
根据坐标图4,计算400K时该反应的平衡常数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为应用广泛的金属单质、B溶液呈浅绿色、C溶液焰色反应呈紫色、C溶液可使酚酞溶液呈红色,各物质有如图所示的相互转化:
试回答:
(1)写出B的化学式 , D的化学式。
(2)写出由E转变成F的化学方程式。
(3)写出向G溶液中加入A的离子方程式:;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成导电高分子材料PPV的反应: ![]()
下列说法正确的是( )
A.合成PPV的反应为加聚反应
B.PPV与聚苯乙烯具有相同的重复结构单元
C.![]() 和苯乙烯互为同系物
和苯乙烯互为同系物
D.通过质谱法测定PPV的平均相对分子质量,可得其聚合度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置能达到实验目的是(夹持仪器未画出)( )
A.
装置用于检验溴丙烷消去产物
B.
装置用于石油的分馏
C.
装置用于实验室制硝基苯
D.
装置可装置证明酸性:盐酸>碳酸>苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列颜色变化与氧化还原反应无关的是( )
A.将乙醇滴入酸性K2Cr2O7溶液中,溶液由橙色变为绿色
B.将SO2通入滴有酚酞的NaOH溶液中,溶液红色褪去
C.将H2C2O4溶液滴入酸性KMnO4溶液中,溶液紫色褪去
D.将乙醛加入新制Cu(OH)2悬浊液中并加热至沸腾,出现红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种形状像布袋结构的烯烃分子Bowtiediene,其形状和结构如下图所示,有关该分子的说法不正确的是( )
A.该烯烃的分子式为C5H4
B.该分子所有碳原子在同一平面
C.1mol该有机物最多可与2molBr2发生加成反应
D.与其互为同分异构体且只含三键的链烃不止一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学对铜与浓硫酸反应产生的黑色沉淀进行探究,实验步骤如下:
Ⅰ.将光亮铜丝插入浓硫酸,加热;
Ⅱ.待产生大量黑色沉淀和气体时,抽出铜丝,停止加热;
Ⅲ.冷却后,从反应后的混合物中分离出黑色沉淀,洗净、干燥备用.
(1)步骤Ⅱ产生的气体是 .
(2)步骤Ⅲ中,“从反应后的混合物中分离出黑色沉淀”的操作是 .
(3)该同学假设黑色沉淀是CuO.检验过程如下:
查阅文献:检验微量Cu2+的方法是:向试液中滴加K4[Fe(CN)6]溶液,若产生红褐色沉淀,证明有Cu2+ .
①将CuO放入稀硫酸中,一段时间后,见明显现象,再滴加K4[Fe(CN)6]溶液,产生红褐色沉淀.
②将黑色沉淀放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,未见红褐色沉淀.
由该检验过程所得结论是 .
(4)再次假设,黑色沉淀是铜的硫化物.实验如下:
实验装置 | 现象 |
| 1A试管中黑色沉淀逐渐溶解 |
①现象2说明黑色沉淀具有性.
②产生红棕色气体的化学方程式是 .
③能确认黑色沉淀中含有S元素的现象是 , 相应的离子方程式是 .
④为确认黑色沉淀是“铜的硫化物”,还需进行的实验是 .
(5)以上实验说明,黑色沉淀中存在铜的硫化物.进一步实验后证明黑色沉淀是CuS与Cu2S的混合物.将黑色沉淀放入浓硫酸中加热一段时间后,沉淀完全溶解,其中CuS溶解的化学方程式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com