
| A. | 烧杯 | B. | 容量瓶 | C. | 蒸馏烧瓶 | D. | 试管 |
科目:高中化学 来源: 题型:选择题
| A. | 醋酸溶液导电性差 | B. | 醋酸溶液中存在醋酸分子 | ||
| C. | 醋酸钠溶液呈碱性 | D. | 0.1 mol/L醋酸溶液的pH=2.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaO+H2O→Ca(OH)2 | B. | 2Na+2H2O→2NaOH+H2↑ | ||
| C. | 2F2+2H2O→4HF+O2 | D. | 2H2+O2$\stackrel{点燃}{→}$2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
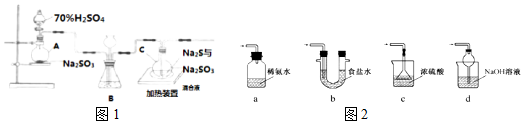
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L CH4含有的共价键数为NA | |
| B. | 1 mol Fe与1mol Cl2充分反应,电子转移数为3NA | |
| C. | 常温下,pH=2的醋酸溶液中含有的H+数目为0.02NA | |
| D. | 常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量 | B. | 密度 | C. | 碳原子数 | D. | 原子总数 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
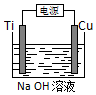 (1)对于Ag2S(s)?2Ag+(aq)+S2-(aq),其Ksp=c(Ag+)2•c(S2-)(写表达式).
(1)对于Ag2S(s)?2Ag+(aq)+S2-(aq),其Ksp=c(Ag+)2•c(S2-)(写表达式).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com