
���� ��1����ҵ����һ����̼��ԭ������������
��2������ˮ������Ӧ����������������������
��3���ڳ�ʪ�Ļ����£���������������ʴ�����������õ������������������ӣ�������ʧȥ�������ɶ��������ӣ���������������ǿ�Ļ�ԭ�����ױ������е�����������������������
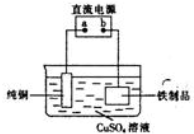
��4��������Ʒ�������һ��ͭ�������ͭ������������������������Ǻ���ͭ���ӵ��Σ����ݵ��صĹ���ԭ�����ش�
��� �⣺��1��һ����̼����������Ӧ�������������̼����ѧ����ʽ��Fe2O3+3CO$\frac{\underline{\;\;��\;\;}}{\;}$2Fe+3CO2��
�ʴ�Ϊ��Fe2O3+3CO$\frac{\underline{\;\;��\;\;}}{\;}$2Fe+3CO2��
��2������ˮ������Ӧ������������������������ѧ����ʽ��3Fe+4H2O$\frac{\underline{\;����\;}}{\;}$Fe3O4+4H2��
�ʴ�Ϊ��3Fe+4H2O$\frac{\underline{\;����\;}}{\;}$Fe3O4+4H2��
��3���ڳ�ʪ�Ļ����£���������������ʴ�����������õ������������������ӣ��缫��ӦʽΪ��O2+4e-+2H2O=4OH-��
������������������ˮ��Ӧ����������������ѧ����ʽ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
O2+4e-+2H2O=4OH-��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��4��������Ʒ�������һ��ͭ�������ͭ���������͵�Դ�����������������������Ϸ�����ԭ��Ӧ����Cu2++2e-=Cu��
�ʴ�Ϊ��������Cu2++2e-=Cu��
���� ���⿼���˻�ѧ����ʽ���缫��Ӧʽ����д����ȷԭ��ء����ع���ԭ���ǽ���ؼ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������ѧ֪ʶ������ش��������⣺
������ѧ֪ʶ������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ca��HCO3��2��Һ�����Ca��OH��2��Һ��Ӧ��Ca2++HCO3-+OH-�TCaCO3��+H2O | |
| B�� | �ö��Ե缫���MgCl2��Һ��2Cl-+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$H2��+Cl2��+2OH- | |
| C�� | ����ͨ��ˮ�У�C12+H2O�T2H++C1-+C1O- | |
| D�� | �����ᱵ��ϡ���ᷴӦ��BaSO3+2H+�TBa2++SO2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���黯ѧ���ʱȽ��ȶ������ܱ��κ����������� | |
| B�� | ��ϩ�ͱ������и�ԭ�Ӷ���ͬһƽ�� | |
| C�� | ��ϩ�ͱ�����ʹ��ˮ��ɫ��������ɫԭ����ͬ | |
| D�� | ʯ�͵��ѻ��������ѽ⣬ú�ĸ����ǻ�ѧ�仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
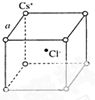
| A�� | �����������������������ȵ�ԭ�� | |
| B�� | M�������ΪK�������һ���ԭ�� | |
| C�� | �������2�����ӵ�ԭ�� | |
| D�� | M��������������ڲ������֮��$\frac{1}{5}$��ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.0 | B�� | 12.3 | C�� | 1.7 | D�� | 12.0 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com