
下面是元素周期表的一部分,参照元素①-⑧在表中的位置,请用化学用语回答下列问题:
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | ⑦ | | | ⑧ | |
(1)Na>Al>O……(2分)
(2)HNO3>H2CO3>H2SiO3 (H4SiO4) ……(2分)
(3)NaOH或NaClO……(2分)
(4)2Mg + CO2 2MgO + C……… (2分)
2MgO + C……… (2分)
(5)2Al + 2OH- + 2H2O =2AlO2- + 3H2↑………(2分)
(6)CH4-8e- +10OH-=CO32- +7H2O………(2分)
(7)CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1 … (2分)
解析试题分析:根据元素在周期表中的位置可知:①为H,②为C,③为N,④为O,⑤为Na,⑥为Al,⑦为Si,⑧为Cl,则
(1)Na、Al位于同一周期,Na原子半径大于Al,O原子核外电子层数最少,原子半径最小,则原子半径:Na>Al>O;
(2)非金属性:N>C>Si,元素的非金属性越强,对应的最高价含氧酸的酸性越强,则酸性:HNO3>H2CO3>H2SiO3。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物为NaOH或NaClO。
(4)由②和④组成的化合物可以是二氧化碳或一氧化碳,⑤的同周期相邻主族元素的单质是镁,镁能与二氧化碳反应生成氧化镁和碳,反应的化学方程式为2Mg + CO2 2MgO + C。
2MgO + C。
(5)⑥单质是铝,与⑤的最高价氧化物的水化物氢氧化钠反应的离子方程式为2Al + 2OH- + 2H2O =2AlO2- + 3H2↑。
(6)①②组成最简单的有机物是甲烷,甲烷作为燃料电池中甲烷在负极通入,所以在碱性介质中燃料电池负极的电极反应式为CH4-8e- +10OH-=CO32- +7H2O。
(7)已知①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ·mol-1、②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ·mol-1,则根据盖斯定律可知(①+②)÷2即得到CH4(g)将NO2(g)还原为N2(g)等的热化学方程式,即CH4(g) +2NO2(g)=N2(g) +CO2(g) +2H2O(g),所以该反应的反应热△H=(-574 kJ·mol-1-1160 kJ·mol-1)÷2=-867 kJ·mol-1。
考点:考查元素周期表和元素周期律的综合应用


科目:高中化学 来源: 题型:填空题
下表为元素周期表的一部分,请回答有关问题:
| | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | | ① | | ② | |
| 3 | | ③ | ④ | ⑤ | | ⑥ | ⑦ | ⑧ |
| 4 | ⑨ | | | | | | ⑩ | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
用
| A.质子数、 | B.中子数、 | C.最外层电子数、 | D.电子层数填写下列空格。 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号)________。
(2)由以上某些元素组成的化合物A、B、C、D有如下转化关系:
A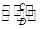 B(在水溶液中进行)
B(在水溶液中进行)
其中C是溶于水显酸性的气体;D是淡黄色固体。
写出C的结构式________;D的电子式________。
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为____________;由A转化为B的离子方程式为_____________________________________________。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因:________________________________________。A、B浓度均为0.1 mol·L-1的混合溶液中,离子浓度由大到小的顺序是__________________;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下表列出了A~R十种元素在周期表中的位置:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | | | | E | R | F | |
| 3 | A | C | D | H | | I | G |
| 4 | B | | | | | | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
Q、W、X、Y、Z为五种原子序数递增的短周期元素。
已知:①Q原子核外电子数等于电子层数,且与W组成的化合物是沼气的主要成分;
②W与Y、X与Y组成的化合物是机动车排出的大气污染物;
③Y与Z能形成电子总数为30和38的两种离子化合物。
(1)W在周期表的位置:________;电子数为38的Y与Z形成化合物的电子式:________。
(2)工业合成XQ3,ΔH<0;下列措施既能加快反应速率,又能使原料转化率一定都提高的是________。
| A.升高温度 |
| B.加入高效催化剂 |
| C.将XQ3及时分离出去 |
| D.增大反应体系压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有X、Y、Z、M四种元素均为短周期元素。有关信息如下表:
(1)X元素在周期表中第_________周期、第_________族;
(2)Y元素的元素符号为_________,1个单质分子中含_________个共用电子对;
(3)Z能在CO2气体中燃烧,其化学反应方程式为_________ 。
(4)化合物X2M3中,各原子(或离子)最外层均达到8电子稳定结构,则X2M3的电子式为 _________,该化合物的水溶液在空气中久置后会被氧化而变质,生成一种单质,所得溶液呈强碱性。用化学方程式表示这个变化过程_________.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
Q、W、X、Y、Z五种短周期元素,原子序数依次增大。Q在元素周期表中原子半径最小,W元素最高正价与最低负价代数和为0;Y与Q同主族;X、Z分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)X、Z简单离子半径较大是 (用离子符号表示)。
(2)由这五种元素中的若干种组成的化合物甲、乙、丙、丁在水溶液中有如下转化关系: ,其中丙是溶于水显酸性的气体,丁是强碱。
,其中丙是溶于水显酸性的气体,丁是强碱。
①若乙常作为焙制糕点的发酵粉,则乙含有的化学键类型有 ;乙溶液中阳离子浓度之和 阴离子浓度之和(填“>”、“=”或“<”)。
②若乙是难溶物,甲溶液与过量的丙生成乙的离子方程式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
周期表中前36号元素A、B、C、D、E、F、G、H,它们的原子序数依次增大,其中B、C、D为同一周期;E、F、G为同一周期;A和E、D和G分别为同一主族;A与B组成的化合物是一种温室气体;D元素原子的最外层电子数是次外层电子数的3倍;E是所在周期原子半径最大的元素(除稀有气体外);F元素的离子半径是同周期元素形成的简单离子中最小的;H元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。
(1)E2D2物质中化学键的类型是__________________
(2)一定条件下,A2气体与C2气体充分反应可生成6.8 g的气体,放出18.44 kJ热量,则该反应的热化学方程式为:_________________________________________;生成物分子的空间构型为_________________,其中C的杂化方式为_______________。
(3)C和E组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是
。
(4)H的基态原子的电子排布式为__________________________已知H2+能与(2)中的生成物的水溶液形成配合物,请写出该配合物中阳离子的结构简式:_________________,在此配合物的水溶液中加入乙醇,现象是_______________________________________。
(5)将足量的GD2通入EDA溶液中所得溶液的离子浓度的大小顺序为:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com