
| A. | S(g)+O2(g)=SO2(g)+Q3 Q3>297.16 kJ | |
| B. | 单斜硫和正交硫互为同分异构体 | |
| C. | 常温下单斜硫比正交硫稳定 | |
| D. | 单斜硫转化为正交硫的反应是吸热反应 |
分析 A.同种物质的气态比固态的能量高;
B.单斜硫和正交硫均为S的单质;
C.①S(s,单斜)+O2(g)=SO2(g)+297.16kJ、②S(s,正交)+O2(g)=SO2(g)+296.83kJ,①-②得S(s,单斜)=S(s,正交)△H=-297.16kJ/mol-(-296.83kJ/mol)<0;
D.△H<0,为放热反应.
解答 解:A.由S(s,单斜)+O2(g)=SO2(g)+297.16kJ,可知为放热反应,S的气态比固态的能量高,则S(g)+O2(g)=SO2(g)+Q3 Q3>297.16 kJ,故A正确;
B.单斜硫和正交硫均为S的单质,二者互为同素异形体,故B错误;
C.①S(s,单斜)+O2(g)=SO2(g)+297.16kJ、②S(s,正交)+O2(g)=SO2(g)+296.83kJ,①-②得S(s,单斜)=S(s,正交)△H=-297.16kJ/mol-(-296.83kJ/mol)<0,则正交硫的能量低,更稳定,故C错误;
D.有选项C中S(s,单斜)=S(s,正交)△H<0,可知为放热反应,故D错误;
故选A.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、盖斯定律应用为解答的关键,侧重分析与应用能力的考查,注意能量低的物质更稳定,题目难度不大.


科目:高中化学 来源: 题型:解答题
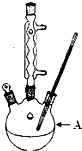 苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)
苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)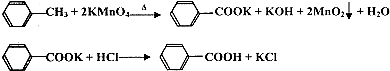
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
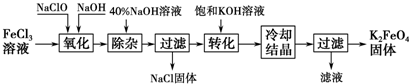
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | H-O | O=O |
| 键能/KJ?mol-1 | 463.4 | 498 |
| A. | 413KJ/mol | B. | 557KJ/mol | C. | 221.6KJ/mol | D. | 436KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
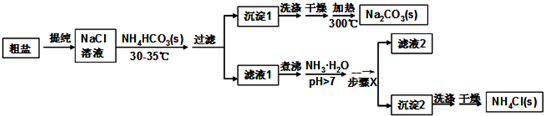
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
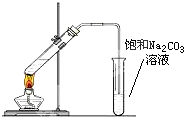 实验室可以用图所示的装置制取乙酸乙酯.回答下列问题:
实验室可以用图所示的装置制取乙酸乙酯.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和热一定是强酸跟强碱反应放出的热量 | |
| B. | 1 mol酸与1 mol碱完全反应放出的热量是中和热 | |
| C. | 在稀溶液中,酸与碱发生中和反应生成1 mol H2O(l)时的反应热叫做中和热 | |
| D. | 表示中和热的离子方程式为:H+(aq)+OH-(aq)=H2O(l)△H=57.3KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com