
【题目】下列实验装置及相应操作正确的是
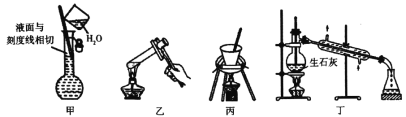
A.图甲可用于配制250ml 0.100mo1/L硫酸溶液时定容操作
B.图乙可用于淀粉在稀硫酸作用下发生水解后,直接滴加新制氢氧化铜悬浊液检验水解产物
C.图丙可用于胆矾结晶水含量测定
D.图丁可用于由工业乙醇制备无水乙醇
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由软锰矿浆(主要成分是MnO2)吸收含硫废渣产生的废气制备,工艺如下图所示。
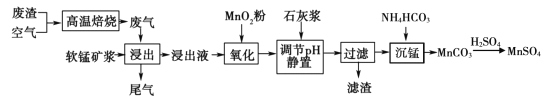
已知:浸出液的pH <2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。请回答下列问题:
(l)高温焙烧前需将矿石研成粉末,其目的是____。
(2)“氧化”中添加适量的MnO2的作用是____(用离子方程式表示);写出“沉锰”的离子方程式____。
(3)下列各组试剂中,能准确测定尾气中SO2含量的是____。(填编号)
a NaOH溶液、酚酞试液
b 稀H2SO4酸化的KMnO4溶液
c 碘水、淀粉溶液
d 氨水、酚酞试液
(4)滤渣的主要成分有____。
(5)若要从MnSO4溶液中得到高纯硫酸锰必须进行的实验操作顺序是____(用字母填空)。
a 过滤洗涤 b 蒸发浓缩 c 冷却结晶 d 干燥
(6)已知:![]() pH =7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于1×10 -6mol/L),需调节溶液pH范围为____
pH =7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于1×10 -6mol/L),需调节溶液pH范围为____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pC类似pH,如图为CO2的水溶液中加入强酸或强碱溶液后,平衡时溶液中各种组分的pC - pH图。依据图中信息,下列说法不正确的是
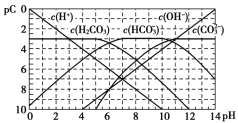
A.![]() 不能在同一溶液中大量共存
不能在同一溶液中大量共存
B.H2CO3电离平衡常数![]()
C.人体血液里主要通过碳酸氢盐缓冲体系(![]() )可以抵消少量酸或碱,维持pH =7.4,但当过量的酸进入血液中时,血液缓冲体系中的
)可以抵消少量酸或碱,维持pH =7.4,但当过量的酸进入血液中时,血液缓冲体系中的![]() 最终将变大
最终将变大
D.pH =9时,溶液中存在关系![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
过渡元素有特殊性能常用于合金冶炼,p区元素用于农药医药、颜料和光电池等工业。
(l)量子力学把电子在原子核外的一种空间运动状态称为一个原子轨道,电子除空间运动状态外,还有一种运动状态叫作_______
(2)基态亚铜离子中电子占据的原子轨道数目为____。
(3)Cr3+可以与CN -形成配离子,其中Cr3+以d2sp3方式杂化,杂化轨道全部用来与CN -形成配位键,则Cr3+的配位数为 ______,1 mol该配离子中含有_______ molσ键。
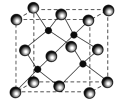
(4)单晶硅可由二氧化硅制得,二氧化硅晶体结构如图所示,在二氧化硅晶体中,Si、O原子所连接的最小环为____元环,则每个O原子连接________个最小环。
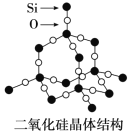
(5)与砷同周期的p区元素中第一电离能大于砷的元素有 ________(填元素符号);请根据物质结构的知识比较酸性强弱亚砷酸(H3AsO3,三元酸)____HNO3(填>,=,<)。
(6) Zn与S形成晶胞结构如图所示,晶体密度为p g/cm3,则晶胞中距离最近的Zn、S之间的核间距离是____pm。(NA表示阿伏加德罗常数,用含p、NA等的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在20.0mL0.10mol·L-1氯水中滴入0.10mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。己知0.10mol·L-1氨水的电离度为1.32%,下列有关叙述正确的是

A. 该滴定过程应该选择酚酞作为指示剂
B. M点对应的盐酸体积为20.0mL
C. M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D. N点处的溶液中pH<12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作或实验现象的解释(方程式)正确的是
A.除去Na2CO3溶液中的Na2SO4,加入适量Ba(OH)2溶液后,过滤:Ba2++![]() =BaSO4↓
=BaSO4↓
B.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2=Ag2S↓+2Cl
C.Na2O2在潮湿的空气中放置一段时间,变成白色黏稠物:2Na2O2+2CO2=2Na2CO3+O2
D.向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀: 2![]() +Ca2++2OH=CaCO3↓+
+Ca2++2OH=CaCO3↓+![]() +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
化学式 | 电离常数 |
|
|
|
|
| |
HF |
|
A.在![]() 酸式盐
酸式盐![]() 溶液中一定存在:
溶液中一定存在:![]()
B.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液中:![]()
C.已知某温度下常见弱酸的电离平衡常数如上表:相同物质的量浓度的![]() 、NaF、
、NaF、![]() 、
、![]() 水溶液,溶液中离子总数由小到大排列的顺序是
水溶液,溶液中离子总数由小到大排列的顺序是![]()
D.pH均等于3的醋酸与盐酸溶液等体积混合后,溶液的pH基本不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知几种物质之间的能量关系如图所示, 下列说法中正确的是
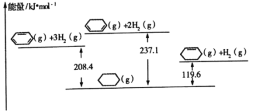
A.使用合适催化剂,能减小反应的焓变
B.![]() +H2(g)
+H2(g)![]()
![]() (g) ΔH=+28.7kJ/mol
(g) ΔH=+28.7kJ/mol
C.![]() (g)中,热能转化为产物内部的能量
(g)中,热能转化为产物内部的能量
D.![]() (g),反应物的总能量低于生成物的总能量
(g),反应物的总能量低于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是世界上产量最大的化学产品之一,乙烯工业是石油化工产业的核心,乙烯产品占石化产品的75%以上,在国民经济中占有重要的地位。有如下两个实验都能用来制备乙烯请根据要求回答问题。
Ⅰ.已知使用活性较低的林德拉催化剂[Pd/(PdO、CaCO3)],可使炔烃的氢化停留在生成烯烃的阶段,而不再进一步氢化成烷烃。现有一课外活动兴趣小组拟由乙炔制得乙烯,并测定乙炔氢化的转化率。若用含0.02mol CaC2的电石和1.600g含杂质18.75 %的锌粒(杂质不与酸反应)分别与足量的X和稀硫酸反应,当反应完全后,测得G中收集到的水VmL(收集到的气体已经转化为标准状况下的体积)。
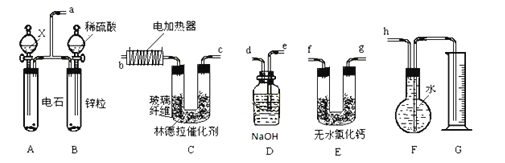
(1)试剂X为:_____。
(2)写出A中所发生反应的化学方程式(有机物写结构简式):_____。
(3)所用装置的连接顺序是_____(填各接口的字母)。
(4)若V=672mL(导管内气体体积忽略不计),则乙炔氢化的转化率为_____。
Ⅱ.实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成 SO2、CO2、水蒸气等无机物。某研究性学习小组用下图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型。
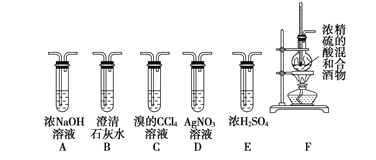
(1)为实现上述实验目的,装置的连接顺序为 F→_____→_____→_____→_____→D。(各装置限用一次),B装置的作用是_____。
(2)当C中观察到_____时,表明单质溴能与乙烯反应;若D中_______,表明C中发生的是取代反应;若D没有出现前面所描述的现象时,表明C中发生的是_____反应,则D装置中溶液的作用_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com