
【题目】往NaOH溶液中加入少量的稀醋酸,若温度不变,下列数据一定增大的是
A.溶液的导电性B.水的离子积C.离子总数D.溶液pH值
 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】制备氮化镁的装置示意图如下: 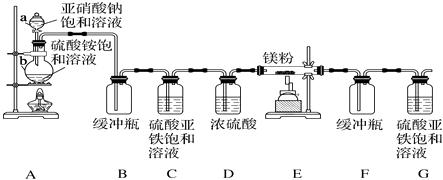
回答下列问题:
(1)仪器a的名称是 , b的名称是 .
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式: .
(3)C的作用是 .
(4)写出E中发生反应的化学方程式: .
(5)请用化学方法确定氮化镁是否含有未反应的镁,写出实验操作及现象 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请填写以下空白:
(1)有以下物质: ①NaHSO4晶体 ②SO3 ③液态硫酸 ④铁 ⑤BaSO4固体 ⑥饱和 FeCl3溶液 ⑦
酒精(C2H5OH) ⑧熔融的 K2SO4,其中能导电的是__________,属于电解质的是_________,属于非电解质的是______________
(2) 化学反应 FeS+ H2SO4(浓)![]() Fe2(SO4)3+ SO2↑+ S↓+ H2O(未配平)中:
Fe2(SO4)3+ SO2↑+ S↓+ H2O(未配平)中:
氧化产物是:_______, 还原产物是:_______。
(3) 请写出醋酸与氢氧化钠溶液反应的离子方程式_______。
(4) 盐酸可以除铁锈, 请写出发生反应的离子方程式_______。
(5) 工业上常用 H2O2在酸性条件下氧化污水中的 Fe2+,请写出离子方程式:_______。
(6)某液态化合物 X2Y4常用作火箭燃料。 32 g X2Y4在一定量的 O2中恰好完全燃烧,反应方程式为: X2Y4(l)+O2(g) ![]() X2(g)+2Y2O(l)。冷却后在标准状况下测得生成物的体积为 22.4 L,其密度为 1.25 g·L-1。 X2的摩尔质量为_____________, X2Y4化学式为________________。(注: l—液态, g—气态)
X2(g)+2Y2O(l)。冷却后在标准状况下测得生成物的体积为 22.4 L,其密度为 1.25 g·L-1。 X2的摩尔质量为_____________, X2Y4化学式为________________。(注: l—液态, g—气态)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于原子核外电子排布的下列叙述不正确的是
A.核外电子总是尽可能排布在能量最低的电子层
B.每一个电子层最多可容纳的电子数为2n2
C.某原子的核外最外层最多可容纳8个电子
D.当M层为次外层时,最多可容纳18个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所涉及的物质均为中学化学中的常见物质,其中D为黄绿色气体,E为Fe,除D、E、C外余化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。
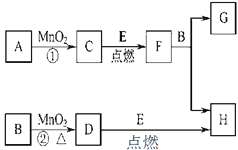
(1)指出MnO2在相关反应中的作用:反应①中是________剂,反应②中是_______剂。
(2)若反应①是在加热条件下进行,则A的化学式是__________;若反应①是在常温条件下进行,则A的化学式是__________。
(3)写出B与MnO2共热获得D的化学方程式_________________________________,该反应中B体现了___________性。
(4)写出F与B反应的离子方程式 ________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com