
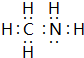 .
.分析 短周期主族元素A、B、C、D的原子序数依次增大,B的化合物种类繁多,数目庞大,故B为C元素;它们的原子核外电子层数之和为7,平均电子层为$\frac{7}{4}$≈1.8,故A有1个电子层,所以A为H元素,则C、D的电子层之和为7-1-2=4,原子序数大于C元素,故二者均为第二周期元素,A与D能形成原子个数比为1:l和2:l的化合物,故D为O元素,C为N元素.
解答 解:短周期主族元素A、B、C、D的原子序数依次增大,B的化合物种类繁多,数目庞大,故B为C元素;它们的原子核外电子层数之和为7,平均电子层为$\frac{7}{4}$≈1.8,故A有1个电子层,所以A为H元素,则C、D的电子层之和为7-1-2=4,原子序数大于C元素,故二者均为第二周期元素,A与D能形成原子个数比为1:l和2:l的化合物,故D为O元素,C为N元素.
(1)人类六大营养素中,只由H、C、O三种元素组成的有糖类、油脂,
只由H、C、O三种元素组成的化合物中,相对分子质量最小的是HCHO,
由H、C、N三种元素按原子数目比5:1:1组成分子E为CH3NH2,其电子式为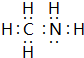 ,
,
故答案为:糖类;HCHO;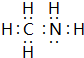 ;
;
(2)由H、N两元素组成的一种常见气态化合物为NH3,其分子的空间构型为三角锥形,工业上合成该气体的化学方程式为:N2+3H2$?_{催化剂}^{高温高压}$2NH3,
故答案为:三角锥形;N2+3H2$?_{催化剂}^{高温高压}$2NH3;
(3)只由H、N、O组成的盐的水溶液显酸性,该盐为NH4NHO3,为强酸弱碱盐,发生水解反应:NH4++H2O?NH3•H2O+H+,
故答案为:NH4++H2O?NH3•H2O+H+;
(4)甲、乙两种化合物都只由H、C、N、O四种元素组成,它们既能与盐酸反应又能与烧碱溶液反应.其中,甲为无机酸式盐,则甲为碳酸氢铵,与烧碱反应的离子方程式是:NH4++HCO3-+OH-=CO32-+NH3.H2O,乙为天然蛋白质水解的相对分子质量最小的产物,乙为氨基乙酸,结构简式为H2NCH2COOH,
故答案为:NH4++HCO3-+OH-=CO32-+NH3.H2O;H2NCH2COOH.
点评 本题以元素推断为载体,考查元素化合物及有机物知识、盐类水解、电子式等,注意充分利用平均电子层推断元素,熟练掌握基础知识.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | CH4、N2、CO2均属于非电解质 | B. | NO2、CO2、H2O均属于氧化物 | ||
| C. | CH4、NO2、CO2均属于非极性分子 | D. | 该反应属于置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol/L的CH3COOH溶液与0.1 mol/L CH3COOH溶液中c(H+)之比为2:1 | |
| B. | 0.1 mol/L NaHCO3溶液中,c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | 0.1 mol/L 的NaHA溶液,其pH=4,则c(HA-)>c(A2-)>c(H2A) | |
| D. | 只含Na+、CH3COO-、H+、OH-的酸性溶液中,c(H+)>c(CH3COO-)>c(Na+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 弱碱的浓度大于强酸的浓度 | |
| B. | 原氨水中有1%的含氮微粒为NH4+ | |
| C. | 反应后的溶液呈酸性 | |
| D. | 混合溶液中c(NH4+)+c(NH3•H2O)+c(NH3)=5×10-4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2 是酸性氧化物,能与NaOH溶液反应 | |
| B. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| C. | Na2O、Na2O2组成元素相同,与 CO2反应产物也相同 | |
| D. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数相等,质量不相等 | B. | 质子数、质量都不相等 | ||
| C. | 分子数、质量分别相等 | D. | 原子数、电子数都相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 图中硬质试管A中放入干燥洁净的细铜丝,烧杯中放入温水,试管B中放入甲醇,右方试管C中放入冷水.向B中不断鼓入空气,使甲醇蒸气和空气通过加热到红热程度的铜丝.
图中硬质试管A中放入干燥洁净的细铜丝,烧杯中放入温水,试管B中放入甲醇,右方试管C中放入冷水.向B中不断鼓入空气,使甲醇蒸气和空气通过加热到红热程度的铜丝.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C60是一种新型的化合物 | |
| B. | C60和石墨都是碳的同素异形体 | |
| C. | C60中虽然没有离子键,但固体为离子晶体 | |
| D. | C60相对分子质量为720 g/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com