
下列说法中正确的是
A.氧化剂本身发生氧化反应
B.氧化还原反应一定有氧元素参加
C.氧化剂在反应中得电子,还原剂失去电子
D.氧化反应一定先于还原反应发生
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源:2014-2015学年广东省东莞市三校高二上学期期中联考化学试卷(解析版) 题型:填空题
(10分)(1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6 kJ的热量,试写出对应的热化学方程式 。
标准状况下11.2L氢气在氯气中充分燃烧放出的热量是 kJ。
(2)A(g)+B(g) C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
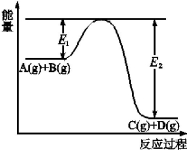
①反应物A(g)和B(g)具有的总能量 (填大于、小于、等于)生成物C(g)和D(g)具有的总能量。
②该反应是_ _反应(填吸热、放热),△H= (用E1和E2表示)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高二12月月考化学试卷(解析版) 题型:填空题
(8分)烷烃分子可以看成由—CH3、—CH2—、 等结合成的。如果某烷分子中同时存在这4种基团,所含碳原子数最小,这种烷烃分子应含 个碳原子,其结构简式可能为 或 或 。
等结合成的。如果某烷分子中同时存在这4种基团,所含碳原子数最小,这种烷烃分子应含 个碳原子,其结构简式可能为 或 或 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高二12月月考化学试卷(解析版) 题型:选择题
已知C4H10的同分异构体有两种:CH3—CH2—CH2—CH3、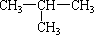 ,则C4H9OH属于醇类的同分异构体共有
,则C4H9OH属于醇类的同分异构体共有
A.l种 B.2种 C.3种 D.4种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省东莞市三校高一上学期期中联考化学试卷(解析版) 题型:实验题
用18mol·L-1的浓H2SO4配制100mL浓度为1.8mol·L-1的H2SO4,其操作可分为以下各步:
a.用量筒量取10.0ml浓H2SO4缓缓注入装有约50mL蒸馏水的烧杯中,并用玻璃棒不断搅拌
b.用约30mL蒸馏水,洗涤烧杯和玻璃棒三次,将每次洗涤液都倒入容量瓶里
c.将稀释后H2SO4冷却到室温后小心转移入容量瓶里
d.检查100mL容量瓶口部是否会发生滴漏
e.将蒸馏水直接加入容量瓶,至液面接近环形刻度线1-2cm处
f.盖紧瓶塞,反复颠倒振荡,摇匀溶液
g.用 向容量瓶里逐滴滴入蒸馏水,至液面最低点恰好和环形刻度线相切
填写下列的空白
(1)步骤C中玻璃棒的作用是
(2)步骤g中空白处所用仪器名称为
(3)正确的操作顺序是(字母填写)
(4)该实验中应选择下列那种规格的容量瓶:
A.150ml B.100ml C.250ml
(5)误差分析,对所配溶液浓度的影响(填偏大,偏小或无影响)
①定容时,俯视刻度线:_____________________
②摇匀后液面低于刻度线后又加水 :_____________________
③配制前,容量瓶壁上有少量水:_______________________
④未洗涤烧杯和玻璃棒:______________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省东莞市三校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列溶液中的氯离子数目与50 mL 1 mol/L的AlCl3溶液中氯离子数目相等的是
A.75 mL 2 mol/L的CaCl2 B.150 mL 1 mol/L的NaCl
C.150 mL 3 mol/L的KCl D.100 mL 2 mol/L的NH4Cl
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高二上学期第二次月考化学试卷(解析版) 题型:填空题
(16分)
化学式 | NH3·H2O | HCN | CH3COOH | H2CO3 |
电离平衡常数(25℃) | Kb=1.77×10-5 | Ka=4.93×10-10 | Ka=1.76×10-5 | Ka1=4.30×10-7 Ka2=5.61×10-11 |
(1)电离平衡常数是衡量弱电解质电离程度强弱的量。上表中给出几种弱电解质的电离平衡常数,从中可以判断:在相同温度下,同浓度的三种酸溶液的导电能力由大到小的顺序为 。
(2)盐类水解程度的强弱同样与弱电解质的电离程度有一定联系,结合表中数据回答下列问题:
①25℃时,有等浓度的a.NaCN溶液、b.Na2CO3溶液、c.CH3COONa溶液,三种溶液的pH由大到小的顺序为 。(填溶液前序号)
②浓度相同的NaCN溶液与CH3COOK溶液相比,c(Na+)-c(CN-) c(K+)-c(CH3COO-)。(填“>”、“<”或“=”)
③将等体积等物质的量浓度的盐酸和氨水混合后,溶液呈 性(填“酸”、“碱”或“中”),用离子方程式表示原因 。
④室温下,若将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液pH随加入盐酸体积的变化曲线如下图所示。b点所示溶液中的溶质是 。
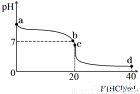
⑤NH4HCO3溶液呈 性(填“酸”、“碱”或 “中”)。
(3)结合表中数据,向NaCN溶液中通入少量CO2,所发生反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高二上学期第二次月考化学试卷(解析版) 题型:选择题
下列事实不能用勒夏特列原理解释的是
A.开启啤酒瓶后,瓶中马上泛起大量泡沫
B.钢铁在潮湿的空气中容易生锈
C.工业上生产硫酸的过程中,二氧化硫在接触室氧化时通入过量空气(O2)
D.工业合成氨时常用通过量氮气的方法提高氢气的转化率
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省蒙自市高二上学期期中化学试卷(解析版) 题型:选择题
下列变化中一定为放热的化学反应的是

A.H2O(g)===H2O(l) ΔH=-44.0 kJ·mol-1
B.N2(g)+O2(g)===2NO(g) ΔH=+182.6 kJ·mol-1
C.形成化学键过程中放出862 kJ热量的化学反应
D.能量变化如上图所示的化学反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com