
ЎҫМвДҝЎҝөӘј°Жд»ҜәПОпФЪ№ӨЕ©ТөЙъІъЎўЙъ»оЦРУРЦШТӘЧчУГЎЈЗл°ҙТӘЗу»ШҙрПВБРПа№ШОКМвЈә
ЈЁ1Ј©Жыіө·ў¶Ҝ»ъ№ӨЧчКұТІ»бТэ·ўN2әНO2·ҙУҰІъЙъҙуЖшОЫИҫОпNOЈ¬ЖдДЬБҝұд»ҜКҫТвНјОӘ
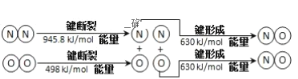
ФтёГ·ҙУҰөДИИ»ҜС§·ҪіМКҪОӘ___ЎЈ
ЈЁ2Ј©№ӨТөәПіЙ°ұөД·ҙУҰЈәN2(g)+3H2(g)![]() 2NH3(g) ЎчH<0Ј¬·ЦұрФЪT1ЎўT2ОВ¶ИПВЈ¬ёДұдЖрКјЗвЖшОпЦКөДБҝЈ¬ІвөГЖҪәвКұ°ұөДМе»э·ЦКэИзНјЛщКҫЈә
2NH3(g) ЎчH<0Ј¬·ЦұрФЪT1ЎўT2ОВ¶ИПВЈ¬ёДұдЖрКјЗвЖшОпЦКөДБҝЈ¬ІвөГЖҪәвКұ°ұөДМе»э·ЦКэИзНјЛщКҫЈә
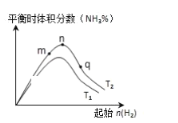
ўЩұИҪПФЪmЎўnЎўqИэөгЛщҙҰөДЖҪәвЧҙМ¬ЦРЈ¬·ҙУҰОпN2өДЧӘ»ҜВКЧоёЯөДКЗ___өгЎЈ
ўЪT2МхјюПВЈ¬ФЪ2LөДГЬұХИЭЖчЦРЈ¬ідИлxmolN2әНymolH2КұЈ¬3minҙпЖҪәвЈ¬ҙЛКұ·ҙУҰОпөДЧӘ»ҜВКҫщОӘaЈ¬РҙіцПВБРҪцә¬aЎўxөДұнҙпКҪЈЁІ»ұШ»ҜјтЈ©Јәv(N2)=___Ј»ёГ·ҙУҰөДЖҪәвіЈКэөДЦөK=___ЎЈ
ўЫНјПсЦРT2___T1ЈЁМоЎ°ёЯУЪЎұЎўЎ°өНУЪЎұЎўЎ°өИУЪЎұ»тЎ°ОЮ·ЁИ·¶ЁЎұЈ©ЎЈ
Ўҫҙр°ёЎҝN2(g)+O2(g)=2NO(g) ЎчH=+183.8kJ/mol q ax/6molЎӨLЈӯ1ЎӨminЈӯ1 16(ax)2/[(x-ax) (3x-3ax)3] өНУЪ
ЎҫҪвОцЎҝ
(1) ЎчH=E(N2)+E(O2)-2E(NO)=945.8kJ/mol+498kJ/mol-2ЎБ630kJ/mol=183.8kJ/mol
ФтёГ·ҙУҰөДИИ»ҜС§·ҪіМКҪОӘN2(g)+O2(g)=2NO(g) ЎчH=+183.8kJ/mol
ҙр°ёОӘN2(g)+O2(g)=2NO(g) ЎчH=+183.8kJ/mol
(2) ўЩ ¶ФУЪN2(g)+3H2(g)![]() 2NH3(g)Ј¬І»¶ПФцҙуH2өДОпЦКөДБҝЈ¬ЖҪәвІ»¶ПХэПтТЖ¶ҜЈ¬·ҙУҰОпN2өДЧӘ»ҜВКІ»¶ПФцҙуЈ¬ЛщТФФЪmЎўnЎўqИэөгЛщҙҰөДЖҪәвЧҙМ¬ЦРЈ¬·ҙУҰОпN2ЧӘ»ҜВКЧоёЯөДөгКЗqөгЎЈҙр°ёОӘq
2NH3(g)Ј¬І»¶ПФцҙуH2өДОпЦКөДБҝЈ¬ЖҪәвІ»¶ПХэПтТЖ¶ҜЈ¬·ҙУҰОпN2өДЧӘ»ҜВКІ»¶ПФцҙуЈ¬ЛщТФФЪmЎўnЎўqИэөгЛщҙҰөДЖҪәвЧҙМ¬ЦРЈ¬·ҙУҰОпN2ЧӘ»ҜВКЧоёЯөДөгКЗqөгЎЈҙр°ёОӘq
ўЪ·ҙУҰОпөДЧӘ»ҜВКҫщОӘaЈ¬ұнГчБҪ·ҙУҰОпөДОпЦКөДБҝЦ®ұИөИУЪ»ҜС§јЖБҝКэЦ®ұИЈ¬јҙy=3x
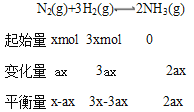
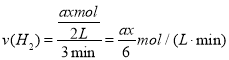 ҙр°ёОӘax/6molЎӨLЈӯ1ЎӨminЈӯ1
ҙр°ёОӘax/6molЎӨLЈӯ1ЎӨminЈӯ1
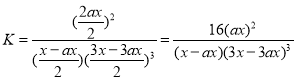 ҙр°ёОӘ16(ax)2/[(x-ax) (3x-3ax)3]
ҙр°ёОӘ16(ax)2/[(x-ax) (3x-3ax)3]
ТтОӘХэ·ҙУҰОӘ·ЕИИ·ҙУҰЈ¬T2Кұ°ұөДМе»э·ЦКэҙуЈ¬ЛөГчОВ¶ИУЙT1ёДұдөҪT2КұЈ¬ЖҪәвХэПтТЖ¶ҜЈ¬ЛщТФНјПсЦРT2<T1ЎЈҙр°ёОӘ <ЎЈ


 ГыРЈҝОМГПөБРҙр°ё
ГыРЈҝОМГПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРЛө·ЁХэИ·өДКЗ( )
A.јЧНйөДұкЧјИјЙХИИОӘ![]() Ј¬ФтјЧНйИјЙХөДИИ»ҜС§·ҪіМКҪҝЙұнКҫОӘЈә
Ј¬ФтјЧНйИјЙХөДИИ»ҜС§·ҪіМКҪҝЙұнКҫОӘЈә![]()
B.ТСЦӘ![]() Ј¬ФтФЪТ»¶ЁМхјюПВПтГЬұХИЭЖчЦРідИл
Ј¬ФтФЪТ»¶ЁМхјюПВПтГЬұХИЭЖчЦРідИл![]()
![]() әН
әН![]()
![]() ід·Ц·ҙУҰәу·Еіц
ід·Ц·ҙУҰәу·Еіц![]() өДИИБҝ
өДИИБҝ
C.![]() КҜД«ЧӘ»ҜОӘ
КҜД«ЧӘ»ҜОӘ![]() КұЈ¬·Еіц
КұЈ¬·Еіц![]() өДИИБҝ
өДИИБҝ![]() (КҜД«Ј¬
(КҜД«Ј¬![]() )
)![]()
D.Н¬ОВН¬С№ПВЈ¬![]() ФЪ№вХХәНөгИјМхјюПВөД
ФЪ№вХХәНөгИјМхјюПВөД![]() І»Н¬
І»Н¬
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ¶МЦЬЖЪФӘЛШWЎўXЎўYЎўZФЪФӘЛШЦЬЖЪұнЦРөДПа¶ФО»ЦГИзұнЛщКҫЈ¬ХвЛДЦЦФӘЛШөДФӯЧУЧоНвІгөзЧУКэЦ®әНОӘ21ЎЈПВБРЛө·ЁІ»ХэИ·өДКЗ

A.ФӯЧУ°лҫ¶ҙуРЎЈәX > Y > Z
B.WЎўYБҪЦЦФӘЛШ¶јДЬУлСхФӘЛШРОіЙ»ҜәПОпWO2ЎўYO2
C.Сх»ҜОп¶ФУҰЛ®»ҜОпөДЛбРФЈә Z > Y > W
D.YДЬРОіЙH2YЎўH2YO4өД»ҜәПОп
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝҪ«Т»¶ЁМе»эөДCO2НЁИлNaOHИЬТәЦРЈ¬ПтЛщөГөДИЬТәAЦРЦрөОјУИл1 molЎӨLЈӯ1өДПЎСОЛбЈ¬ЛщјУСОЛбөДМе»эУлІъЙъCO2өДМе»э№ШПөИзНјЛщКҫЈә
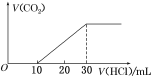
ИЬТәAЦРөДИЬЦККЗЈЁ Ј©ЎЈ
A.Na2CO3әНNaHCO3B.NaOHәНNa2CO3C.Na2CO3D.NaHCO3
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝМъј°МјөД»ҜәПОпФЪЙз»бЙъІъЎўЙъ»оЦРУРЧЕ№г·әөДУҰУГЎЈЗл»ШҙрПВБРОКМвЈә
ЈЁ1Ј©ҙЕМъҝуКЗ№ӨТөЙПТұБ¶МъөДФӯБПЦ®Т»ЎЈ
ТСЦӘЈәўЩFe3O4ЈЁsЈ©+4CЈЁsЈ©![]() 3FeЈЁsЈ©+4COЈЁgЈ© ЎчH=+646.0kJmol©Ғ1
3FeЈЁsЈ©+4COЈЁgЈ© ЎчH=+646.0kJmol©Ғ1
ўЪCЈЁsЈ©+CO2ЈЁgЈ©2COЈЁgЈ© ЎчH=+172.5kJmol©Ғ1
ФтFe3O4ЈЁsЈ©+4COЈЁgЈ©![]() 3FeЈЁsЈ©+4CO2ЈЁgЈ©ЎчH=___ЎЈ
3FeЈЁsЈ©+4CO2ЈЁgЈ©ЎчH=___ЎЈ
ЈЁ2Ј©·ҙУҰFeЈЁsЈ©+CO2ЈЁgЈ©![]() FeOЈЁsЈ©+COЈЁgЈ©ЎчHөДЖҪәвіЈКэОӘKЈ¬ФЪІ»Н¬ОВ¶ИПВЈ¬KЦөИзПВЈә
FeOЈЁsЈ©+COЈЁgЈ©ЎчHөДЖҪәвіЈКэОӘKЈ¬ФЪІ»Н¬ОВ¶ИПВЈ¬KЦөИзПВЈә
ОВ¶И/K | 973 | 1173 | 1373 | 1573 |
K | 1.47 | 2.15 | 3.36 | 8.92 |
ўЩҙУұнЦРКэҫЭҝЙНЖ¶ПЈ¬ёГ·ҙУҰКЗ___ЈЁМоЎ°·ЕИИЎұ»тЎ°ОьИИЎұЈ©·ҙУҰЎЈ
ўЪОВ¶ИОӘ973KКұЈ¬ФЪДіәгИЭГЬұХИЭЖчЦР·ўЙъЙПКц·ҙУҰЎЈПВБРУР№ШЛө·ЁДЬЛөГчёГ·ҙУҰТСҙпөҪЖҪәвЧҙМ¬өДКЗ___ЈЁМоЧЦДёЈ©ЎЈ
AЈ®cЈЁCO2Ј©=cЈЁCOЈ©
BЈ®vХэЈЁCO2Ј©=vДжЈЁCOЈ©
CЈ®МеПөС№ЗҝІ»ұд
DЈ®»мәПЖшМеЦРcЈЁCOЈ©І»ұд
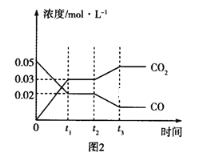
ЈЁ3Ј©ИзНјНј1Ўў2ұнКҫ·ҙУҰЈәH2ЈЁgЈ©+CO2ЈЁgЈ©![]() COЈЁgЈ©+H2OЈЁgЈ©ЎчHЈҫ0УР№ШБҝУл·ҙУҰКұјдЦ®јдөД№ШПөЈә
COЈЁgЈ©+H2OЈЁgЈ©ЎчHЈҫ0УР№ШБҝУл·ҙУҰКұјдЦ®јдөД№ШПөЈә
ўЩНј2ЦРИфt1=0.5minЈ¬Фт0Ў«t1Кұјд¶ОДЪЈ¬H2OөДЖҪҫщ·ҙУҰЛЩВКvЈЁH2OЈ©=___molL©Ғ1s©Ғ1ЎЈ
ўЪНј1ЦРt2КұҝМёДұдөДМхјюКЗ___ЈЁИОРҙБҪЦЦЈ¬ПВН¬Ј©Ј»Нј2ЦРt2КұҝМёДұдөДМхјюКЗ___ЎЈ

Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ·ҙУҰ![]() ФЪТ»ёцГЬұХИЭЖчЦРҪшРРЈ¬ПВБРҙлК©ҝЙТФК№·ҙУҰЛЩВКФцҙуөДКЗЈЁ Ј©
ФЪТ»ёцГЬұХИЭЖчЦРҪшРРЈ¬ПВБРҙлК©ҝЙТФК№·ҙУҰЛЩВКФцҙуөДКЗЈЁ Ј©
ўЩФцјУЙЩБҝ![]() ўЪЙэёЯОВ¶ИўЫМе»эІ»ұдЈ¬ФЩНЁИл
ўЪЙэёЯОВ¶ИўЫМе»эІ»ұдЈ¬ФЩНЁИл![]() ўЬЛхРЎМе»эФцҙуС№ЗҝўЭМе»эІ»ұдЈ¬ФЩНЁИлHeўЮС№ЗҝІ»ұдЈ¬ФЩНЁИлHe
ўЬЛхРЎМе»эФцҙуС№ЗҝўЭМе»эІ»ұдЈ¬ФЩНЁИлHeўЮС№ЗҝІ»ұдЈ¬ФЩНЁИлHe
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ¶МЦЬЖЪЦчЧеФӘЛШWЎўXЎўYЎўZөДФӯЧУРтКэТАҙОФцјУЈ¬ҪцXЎўYҙҰУЪН¬ЦЬЖЪЈ¬YКЗөШҝЗЦРә¬БҝЧоёЯөДФӘЛШЈ¬ZөДФӯЧУРтКэКЗXөДБҪұ¶Ј¬XУлYРОіЙөД»ҜәПОпҝЙУлZөДөҘЦК·ҙУҰЙъіЙXөДөҘЦКЎЈПВБРЛө·ЁХэИ·өДКЗ( )ЎЈ
A.јтөҘАлЧУөД°лҫ¶Јә![]()
B.јтөҘЗв»ҜОпөДИИОИ¶ЁРФЈә![]()
C.WУлYРОіЙөД»ҜәПОпЦ»ә¬УРј«РФ№ІјЫјь
D.ZөДЧоёЯјЫСх»ҜОп¶ФУҰөДЛ®»ҜОпОӘЗҝјо
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝҪ«2.32gNa2CO3ЎўNaOHөД№ММе»мәПОпНкИ«ИЬҪвУЪЛ®Ј¬ЦЖіЙИЬТәЈ¬И»әуПтёГИЬТәЦРЦрөОјУИл1mol/LөДСОЛбЈ¬ЛщјУСОЛбөДМе»эУлІъЙъCO2өДМе»э(ұкЧјЧҙҝц) №ШПөИзНјЛщКҫЈ¬ПВБРЛө·ЁЦРҙнОуөДКЗЈЁ Ј©
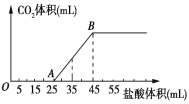
A.OA¶О·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪОӘЈәH++OH-=H2OЎўCO32-+H+=HCO3-
B.AөгИЬТәЦРөДИЬЦКОӘNaClЎўNaHCO3
C.»мәПОпЦРNaOHөДЦКБҝ0.60g
D.өұјУИл35mLСОЛбКұЈ¬ІъЙъCO2өДМе»эОӘ224mL
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝXЎўYЎўZәНWҙъұнФӯЧУРтКэТАҙОФцҙуөДЛДЦЦ¶МЦЬЖЪФӘЛШЈ¬ЛьГЗВъЧгТФПВМхјюЈә
ўЩФӘЛШЦЬЖЪұнЦРЈ¬ZУлYПаБЪЈ¬ZУлWТІПаБЪЈ»ўЪYЎўZәНWИэЦЦФӘЛШөДФӯЧУЧоНвІгөзЧУКэЦ®әНОӘ17ЎЈ
ЗлМоҝХЈә
ЈЁ1Ј©YЎўZәНWКЗ·сО»УЪН¬Т»ЦЬЖЪЈЁМоЎ°КЗЎұ»тЎ°·сЎұЈ©Јә__________Ј¬АнУЙКЗ________________ЎЈ
ЈЁ2Ј©YКЗ_______Ј¬ZКЗ_______Ј¬WКЗ_______ЎЈ
ЈЁ3Ј©XЎўYЎўZәНWҝЙЧйіЙТ»ЦЦ»ҜәПОпЈ¬ЖдФӯЧУёцКэұИОӘ8ЎГ2ЎГ4ЎГ1Ј¬РҙіцёГ»ҜәПОпөДГыіЖј°»ҜС§КҪЈә _______________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com