
| A. | 碳酸钙受热分解 | B. | 乙醇燃烧 | ||
| C. | 铝粉与盐酸的反应 | D. | 氧化钙溶于水 |
分析 生成物总能量高于反应物总能量的反应属于吸热反应,根据常见的放热反应和吸热反应进行判断.若反应物的总能量大于生成物的总能量则为放热反应.
常见的放热反应有:所有的物质燃烧、所有金属与酸、所有中和反应、绝大多数化合反应,铝热反应;
常见的吸热反应有:个别的化合反应(如C和CO2)、绝大数分解反应、少数分解置换以及某些复分解(如铵盐和强碱).
解答 解:A.碳酸钙受热分解属于吸热反应,生成物总能量高于反应物总能量,故A正确;
B.乙醇燃烧属于放热反应,生成物的总能量小于反应物的总能量,故B错误;
C.铝与盐酸反应属于放热反应,生成物的总能量小于反应物的总能量,故C错误;
D.氧化钙溶于水与水发生化合反应,属于放热反应,生成物的总能量小于反应物的总能量,故D错误.
故选A.
点评 本题主要考查了放热反应和放热反应,题目难度不大,掌握常见的放热反应和放热反应是解题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | 除⑤外 | C. | 除①外 | D. | 除①、⑤外 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;DB2有多种重要的用途,请你写出其中的一种:制玻璃、制光导纤维、制粗硅(其中一种).
;DB2有多种重要的用途,请你写出其中的一种:制玻璃、制光导纤维、制粗硅(其中一种).查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,B中具有的官能团的名称酯基、溴原子.
,B中具有的官能团的名称酯基、溴原子.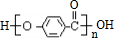 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | X | Y | Z | W |
| 相关信息 | 短周期p区元素,有种单质常作电极材料 | 基态原子2p能级上各轨道中均有电子且电子的自旋方向相同 | 基态原子的核外电子共有17种运动状态 | 位于第四周期第VA族 |
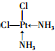 (YH3作为一个整体写)
(YH3作为一个整体写)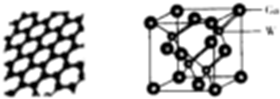
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+(aq)+$\frac{1}{2}$SO42-(aq)+$\frac{1}{2}$Ba2+(aq)+OH-(aq)═$\frac{1}{2}$BaSO4(s)+H2O(1);△H=-57.3 kJ/mol | |
| B. | KOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$K2SO4(aq)+H2O(l);△H=-57.3kJ/mol | |
| C. | C8H18(l)+$\frac{25}{2}$O2 (g)═8CO2 (g)+9H2O(g);△H=-5518 kJ/mol | |
| D. | 2C8H18(g)+25O2 (g)═16CO2 (g)+18H2O(1);△H=-5518 kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com