
某化学兴趣小组按照下列方案进行“由含铁废铝制备硫酸铝晶体”的实验:
步骤1:取一定量含铁废铝,加足量的NaOH溶液,反应完全后过滤。
步骤2:边搅拌边向滤液中滴加稀硫酸至溶液的pH=8~9,静置、过滤、洗涤。
步骤3:将步骤2中得到的固体溶于足量的稀硫酸。
步骤4: 。
请回答以下问题:
(1)上述实验中的过滤操作需要玻璃棒、 等玻璃仪器。
(2)步骤1发生反应的离子方程式为
过滤的目的是__________________________________________。
(3)当步骤2中的溶液pH=8~9时,检验沉淀是否完全的方法是______________。
(4)步骤2中溶液的pH控制较难操作,可改用____________________,发生反应的离子方程式为 。
(5)步骤4的操作为 。
【知识点】铝的重要性质 实验操作 C2 J1 J2
【答案解析】(1)烧杯、漏斗 (2)略,除去铁等不溶于碱的杂质
(3)取上层清液,逐滴加入稀硫酸,若变浑浊则说明沉淀不完全,若不变浑浊则说明沉淀完全
(4)通入足量CO2气体,略
(5)将得到的溶液蒸发浓缩、冷却、结晶、过滤、干燥
解析::(1)过滤操作中需要大小烧杯各一个、漏斗、玻璃棒,因此过滤操作中需要的玻璃仪器有:烧杯、漏斗、玻璃棒;
(2)Al能与氢氧化钠溶液反应生成偏铝酸钠和氢气,化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
Al能与氢氧化钠溶液反应,铁不能与氢氧化钠溶液反应,通过过滤将杂质铁从溶液中除掉,
(3)检验沉淀是否完全的方法是取上层清液,逐滴加入稀硫酸,若变浑浊则说明沉淀不完全,若不变浑浊则说明沉淀完全。
(4)边搅拌边向滤液中滴加稀硫酸至溶液的pH=8~9,目的是生成氢氧化铝,可利用往偏铝酸钠溶液中通入足量CO2气体的方法,不必控制溶液的PH就可得到最大量的沉淀。
(5)步骤3:将步骤2中得到的固体溶于足量的稀硫酸得到硫酸铝溶液,将得到的溶液蒸发浓缩、冷却、结晶、过滤、干燥得晶体。
【思路点拨】本题考查了铝的重要性质和实验操作,掌握铝能与强碱性溶液反应而铁不与强碱性溶液反应是关键。


科目:高中化学 来源: 题型:
A、B两种烃的最简式相同,7.8 g A完全燃烧后生成物通入过量的石灰水中,得到沉淀60 g。既可以用酸性KMnO4溶液对A、B进行鉴别,也可以用溴水反应对它们进行鉴别。0.5 mol B完全燃烧生成22.4 L CO2(标准状况)和9 g水,在相同状况下,A与B蒸气的密度比为3∶1。试通过计算推断这两种烃的结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出下列化合物的名称或结构简式:
①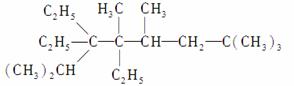
________________________________________________________________________,
②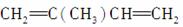 ________________________________________________________________________,
________________________________________________________________________,
③CH2===CHCOOH________________________________________________________________________,
④2,5二甲基 2,4己二烯的结构简式:
________________________________________________________________________
________________________________________________________________________。
(2)麻黄素又称黄碱,是我国特定的中药材麻黄中所含有的一种生物碱,经我国科学家研究发现其结构如下: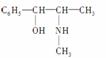
①麻黄素中含氧官能团的名称是________,属于________类(填“醇”或“酚”)。
②下列各物质:
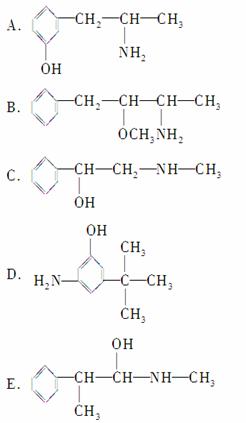
与麻黄素互为同分异构体的是________(填字母,下同),互为同系物的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下述实验不能达到预期实验目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 将2.5 g CuSO4·5H2O溶解在97.5 g 水中 | 配制质量分数为1.6%的CuSO4溶液 |
| B | 向盛有1 mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C | 取少量待检固体溶于水中,滴加少量Ba(OH)2溶液,观察是否有白色沉淀生成 | 检验NaHCO3固体中是否含Na2CO3 |
| D | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体从分液漏斗上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某固体粉末甲中可能含有K2CO3、KNO3、NaNO2、K2SO3、Na2SO4、FeO、Fe2O3中的若干种,某同学为确定该固体粉末的成分,取甲进行连续实验,实验过程及现象如下 ,该同学得出的结论正确的是( )
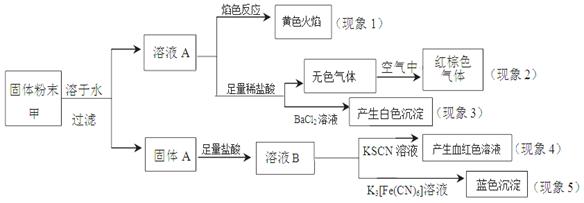
A.根据现象1可推出该固体粉末中含有钠元素,但不含钾元素
B.根据现象2可推出该固体粉末中一定含有NaNO2
C.根据现象3可推出该固体粉末中一定含有Na2SO4
D.根据现象4和现象5可推出该固体粉末中一定含有FeO和Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
铜等金属及其化合物在日常生产生活中用途非常广泛。
Ⅰ.孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物,实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:
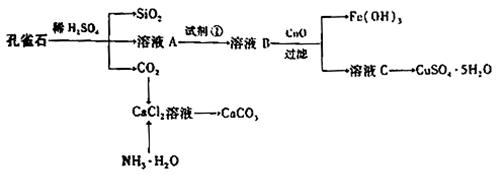
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+:从下列所给试剂中选择:实验步骤中试剂①为 (填代号),检验溶液A中Fe3+的最佳试剂为 (填代号)。
a.KMnO4 b. (NH4) 2S c. H2O2 d.KSCN
(2)由溶液C获得CuSO4·5H2O,需要经过 等操作。
(3)制备CaCO3时,应向CaCl2溶液中选通入(或先加入) (填化学式)。若实验过程中有氨气逸出、应选用下列 装置回收(填代号)。
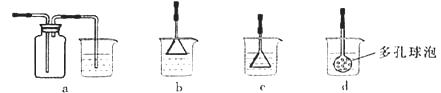
Ⅱ.(1)某同学欲从含FeCl3、FeCl2、CuCl2的废液中回收金属铜,取上述1L废液加入铁粉,充分反应。所加铁粉的物质的量与废液中铜离子的物质的量的关系曲线如图:
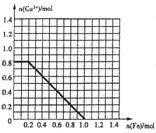 已知原废液中c(Cl-)=6.0mol.L-1,则原废液中c(Fe3+)= ,c(Fe2+)= 。(忽略水解及溶液体积变化)
已知原废液中c(Cl-)=6.0mol.L-1,则原废液中c(Fe3+)= ,c(Fe2+)= 。(忽略水解及溶液体积变化)
(2)现有Fe2O3、ZnO、CuO的混合固体粉末ag,在加热条件下用足量的CO还原,得到金属混合物2.41g,将生成的CO2气体用足量的澄清石灰水吸收后,产生5.00g白色沉淀。请回答下列问题:
①a= 。
②若agFe2O3、ZnO、CuO的混合物总物质的量为bmol,则Fe2O3的物质的量为 。(用含b的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色
B.有机物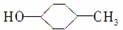 的消去产物有两种
的消去产物有两种
C.有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是

D.可用溴水鉴别甲苯、苯酚、1己烯三种无色液体
D [甲苯只能使酸性高锰酸钾溶液褪色而不能使溴的四氯化碳溶液褪色;有机物有如下对称轴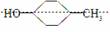 ,其消去产物只有一种;有机物
,其消去产物只有一种;有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
有FeO、Fe2O3的混合物若干克,在足量H2气流中,加热充分反应,冷却后称得剩余固体比原混合物减轻0.8g;将等质量的原混合物与盐酸反应,欲使之完全溶解,需1 mol·L-1的盐酸的体积至少为
A.0.05 L B.0.1 L C.0.2 L D.1 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com