
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | c(H+) 增大 | B. | Ka(HF)增大 | C. | $\frac{c({F}^{-})}{c({H}^{+})}$减小 | D. | $\frac{c({H}^{+})}{c(HF)}$减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
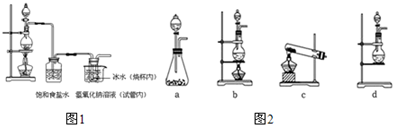
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去乙醇中微量水用金属钠 | |
| B. | 溴苯中混有溴,加入水萃取 | |
| C. | 用酸性高锰酸钾除去乙烷中的乙烯 | |
| D. | 除去乙醇中少量的乙酸:加足量生石灰,蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的还原产物是 I2 | |
| B. | 每生成 1 mol I2,转移的电子为 2 mol | |
| C. | KOH 和 O2 都是还原产物 | |
| D. | 反应中氧化剂与还原剂质量之比为 1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1 mol金属钠变为钠离子时失去的电子数为NA | |
| B. | 在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10 NA | |
| C. | 0.1mol/L的MgCl2溶液中,含有Mg2+数目为0.1NA | |
| D. | 常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L乙醇中含有的氧原子数为NA | |
| B. | 64g的S2和S8混合物中,含硫原子总数为2 NA | |
| C. | 1L 1mol/L氯化铁溶液中,含有NA个Fe3+ | |
| D. | 25℃时,pH=13的Ba(OH)2溶液中含有OH-数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com