
| A. | 某烷烃的名称为2,2,4,4-四甲基-3,3,5-三乙基己烷 | |
| B. | 等质量的甲醛与乳酸[CH3CH(OH)COOH]完全燃烧消耗氧气的量不相等 | |
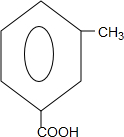
| C. | 如图是某有机物分子的比例模型,该物质可能是一种氨基酸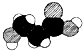 | |
| D. | 化合物 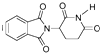 在酸性条件下水解,所得溶液加碱后加热有NH3生成 在酸性条件下水解,所得溶液加碱后加热有NH3生成 |
分析 A、己烷命名中5号碳出现乙基,说明选取的不是最长碳链;
B、醛和乳酸的最简式相同,等质量的二者完全燃烧时消耗的氧气的量相同;
C、 ,该模型中出现三种元素,应为羟基丙酸;
,该模型中出现三种元素,应为羟基丙酸;
D、该化合物中含有肽键,酸性条件下水解生成铵离子,加碱溶液后加热,铵离子与氢氧根离子反应成氨气.
解答 解:A、2,2,4,4-四甲基-3,3,5-三乙基己烷,最长碳链应为7,正确命名应该为2,2,4,4,5-五甲基-3,3-二乙基-庚烷,故A错误;
B、甲醛分子式CH2O,乳酸的最简式为CH2O,所以等质量的甲醛与乳酸[CH3CH(OH)COOH]完全燃烧消耗氧气的量相等,故B错误;
C、 ,该模型中出现三种元素,应为羟基丙酸,不是氨基酸,故C错误;
,该模型中出现三种元素,应为羟基丙酸,不是氨基酸,故C错误;
D、化合物 在酸性条件下水解产物中含有铵离子,然后在碱性溶液中加热,铵离子与氢氧根离子反应生成氨气,故D正确;
在酸性条件下水解产物中含有铵离子,然后在碱性溶液中加热,铵离子与氢氧根离子反应生成氨气,故D正确;
故选D.
点评 本题考查了有机物的命名,题目难度不大,该题注重了基础性试题的考查,侧重对学生基础知识的检验和训练,该题的关键是明确有机物的命名原则,然后结合有机物的结构简式灵活运用即可,有利于培养学生的规范答题能力.


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源: 题型:解答题
 ;A在一定条件下能与水反应,可用于饮用水的消毒,试写出此反应的化学反应方程式NCl3+3H2O=NH3+3HClO.
;A在一定条件下能与水反应,可用于饮用水的消毒,试写出此反应的化学反应方程式NCl3+3H2O=NH3+3HClO.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
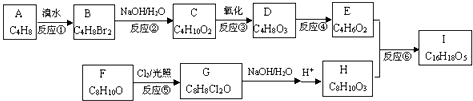
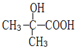 .
.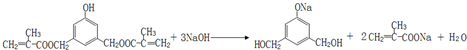 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
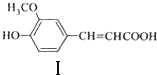 的说法,正确的是AB.
的说法,正确的是AB.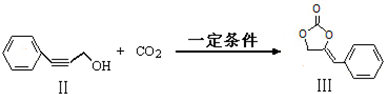
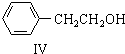 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$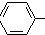 CH2CH2
CH2CH2 -CH2CH3+H2O
-CH2CH3+H2O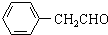 ;
;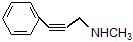 也可以和CO2发生类似反应①的反应,生成由VI,VI的结构简式为
也可以和CO2发生类似反应①的反应,生成由VI,VI的结构简式为 .
. .
.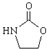 ,涉及的反应方程式为HOCH2CH2NH2+CO2$\stackrel{催化剂}{→}$
,涉及的反应方程式为HOCH2CH2NH2+CO2$\stackrel{催化剂}{→}$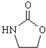 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
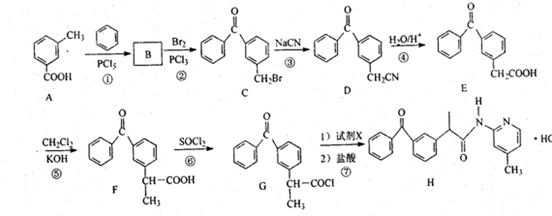
 +
+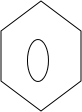 $\stackrel{PCl_{3}}{→}$
$\stackrel{PCl_{3}}{→}$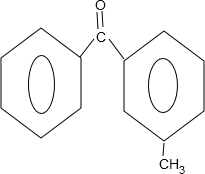 +H2O.
+H2O.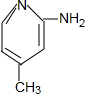 .
.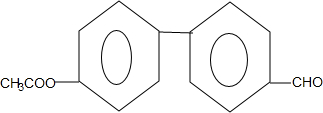 (只写一种).
(只写一种).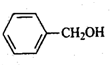 和
和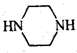 为原料制备
为原料制备 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
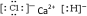 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
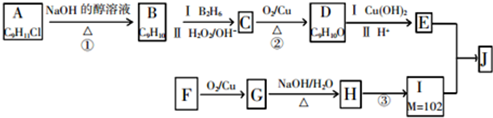
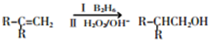
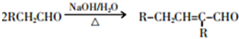
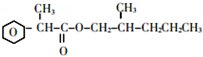 .
.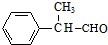 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$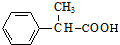 +Cu2O↓+2H2O.
+Cu2O↓+2H2O.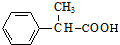 +CH3CH2CH2CH2CH(CH3)OH$→_{△}^{浓硫酸}$
+CH3CH2CH2CH2CH(CH3)OH$→_{△}^{浓硫酸}$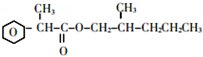 +H2O.F→G的化学方程式2CH3CH2CH2OH+O2$→_{△}^{Cu}$2CH3CH2CHO+2H2O.
+H2O.F→G的化学方程式2CH3CH2CH2OH+O2$→_{△}^{Cu}$2CH3CH2CHO+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向CuSO4溶液中滴加氨水,先生成深蓝色溶液,后生成蓝色沉淀 | |
| B. | 向NH4Fe(SO4)2溶液中滴加少量NaOH溶液,NH4+先发生反应 | |
| C. | 向等浓度的FeCl3和CuCl2混合溶液中加入少量Fe粉,Cu2+先被还原 | |
| D. | 足量锌与浓硫酸反应,先产生二氧化硫,后产生氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
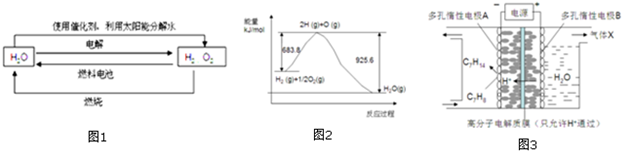
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com