
【题目】一定条件下反应2AB(g) ![]() A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A. 容器内压强不随时间变化B. 容器内,3种气体AB、A2、B2共存
C. 容器中各组分的体积分数不随时间变化D. AB的消耗速率等于A2的消耗速率
【答案】C
【解析】
化学反应达到平衡状态有两大特征,即正反应与逆反应的速率相等、各组分浓度保持不变。由此可以直接或间接地衍生出以下5种判断方式:
(1)从速率的角度描述:同一物质的生成速率等于消耗速率;处于同一可逆方程式中的不同物质,其正反应速率与逆反应速率之比等于化学计量数之比;
(2)反应混合物中各物质的物质的量分数、质量分数、体积分数(对气体物质而言)等保持不变;
(3)反应混合物中某一种反应物的转化率、某一生成物的产率等保持不变;
(4)反应混合物中某些特征,如某组分的颜色、体系的颜色不再改变;
(5)对于mA(g)+nB(g) ![]() pC(g)+qD(g) (其中m+n≠p+q)的可逆反应而言:定温、定容条件下,总压强保持不变;定温、定压条件下,总体积保持不变;总物质的量保持不变;总分子数保持不变等。
pC(g)+qD(g) (其中m+n≠p+q)的可逆反应而言:定温、定容条件下,总压强保持不变;定温、定压条件下,总体积保持不变;总物质的量保持不变;总分子数保持不变等。
A. 因反应前后气体分子数相等,因此容器内压强不随时间而变化,不能用作判断反应达到平衡状态的标志,A项错误;
B. 在可逆反应中,因反应不能进行彻底,因此容器内3种气体始终共存,不能用作判断反应达到平衡状态的标志,B项错误;
C. 容器中各组分的体积分数不随时间变化,说明各组分浓度保持不变,可以用作判断反应达到平衡状态的标志,C项正确;
D.由于AB与A2的化学计量数之比为2:1,因此当达到平衡时AB的消耗速率与A2的消耗速率之比应为2:1,D项错误;
答案应选C。


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1mol铵根离子中含有的电子数为9NA
B.38.5gCCl4中含有的共用电子对数为NA
C.16gO3单质中含有的分子个数为NA
D.通常状况下,11.2 LCl2通入足量的NaOH溶液中,转移的电子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂碳、铝、铬是重要的元素,在工业生产和科技中有重要的应用。
(1)铝热反应可以冶炼金属铬,Cr基态核外电子排布式为_____________。
(2)金属锂是锂电池重要的组成部分。Li、Be、B 原子的第一电离能由大到小的顺序为______。
(3)LiAlH4是有机合成中常用的还原剂。AlH4-的空间构型为___________。
(4)![]() +
+
![]()
![]() +CH3COOH
+CH3COOH
①乙酸酐分子中碳原子轨道的杂化类型为________。
②l mol对甲基苯乙酮分子中含有的σ键的数目为_______
③甲苯分子难溶于水的原因是________。
(5)已知铬酸钙晶胞如图所示,该晶体密度为ρ g·cm-1,NA是阿伏加德罗常数的值。Ca离子周围距离最近且相等的O有_____个。相邻两个面心氧离子最短核间距(d)为_______pm。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物![]() (X)、
(X)、![]() (Y)、
(Y)、![]() (Z)的分子式均为C5H6。下列说法正确的是( )
(Z)的分子式均为C5H6。下列说法正确的是( )
A.X、Y、Z均能使酸性高锰酸钾溶液褪色
B.Z的同分异构体只有X和Y两种
C.Z的二氯代物只有两种(不考虑立体异构)
D.Y分子中所有碳原子均处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计了一种智能双模式海水电池,满足水下航行器对高功率和长续航的需求。负极为Zn,正极放电原理如图。下列说法错误的是( )
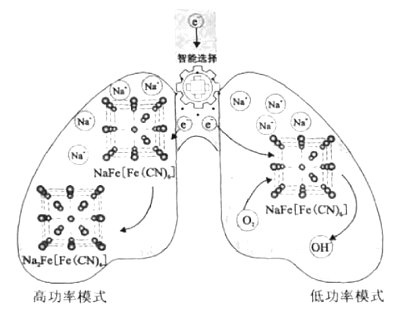
A. 电池以低功率模式工作时,NaFe[Fe(CN)6]作催化剂
B. 电池以低功率模式工作时,Na+的嵌入与脱嵌同时进行
C. 电池以高功率模式工作时,正极反应式为:NaFe[Fe(CN)6]+e-+Na+=Na2Fe[Fe(CN)6]
D. 若在无溶解氧的海水中,该电池仍能实现长续航的需求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟代硼酸钾(KBe2BO3F2)是激光器的核心材料,我国化学家在此领域的研究走在了世界的最前列。回答下列问题:
(1)氟代硼酸钾中非金属元素原子的电负性大小顺序是__。基态K+的电子排布式为__。
(2)NaBH4是有机合成中常用的还原剂,其中的阴离子空间构型是__,中心原子的杂化方式为__。NaBH4中存在__(填标号)。
a.离子键 b.氢键 c.σ键 d.π键
(3)BeCl2中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的BeCl2的结构式为__,其中Be的配位数为__。
(4)第三周期元素氟化物的熔点如下表:
化合物 | NaF | MgF2 | AlF3 | SiF4 | PF5 | SF6 |
熔点/℃ | 993 | 1261 | 1291 | -90 | -83 | -50.5 |
解释表中氟化物熔点变化的原因:___。
(5)CaF2的一种晶胞如图所示。Ca2+占据F-形成的空隙,若r(F-)=xpm,r(Ca2+)=ypm,设阿伏加德罗常数的值为NA,则CaF2的密度ρ=__g·cm-3(列出计算表达式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯分子结构的说法中,错误的是( )
A.各原子均位于同一平面上,6个碳原子彼此连接成为一个平面正六边形的结构
B.苯环中含有3个C—C单键,3个![]() 双键
双键
C.苯分子中6个碳碳键完全相同
D.苯分子中碳碳之间的键是介于单键和双键之间特殊的键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见有机反应类型有:①取代反应、②加成反应、③消去反应、④酯化反应、⑤加聚反应、⑥氧化反应、⑦还原反应,其中能在有机物中引入羟基的反应类型是
A. ①②③B. ①②⑦C. ⑤⑥⑦D. ③④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com