
| Ń”Ļī | ŹµŃé²Ł×÷ÓėĻÖĻó | ½āŹĶ»ņ½įĀŪ |
| A | ¹żĮæµÄĢś·ŪÖŠ¼ÓČėĻ”ĻõĖįÖŠ£¬³ä·Ö·“Ó¦ŗ󣬵ĪČėKSCNČÜŅŗ£¬ČÜŅŗ³ŹŗģÉ« | Ļ”ĻõĖį½«FeŃõ»ÆĪŖFe3+ |
| B | AgI¹ĢĢåÖŠµĪČėKClČÜŅŗ£¬³ĮµķÓÉ»ĘÉ«±äĪŖ°×É« | AgI±ČAgClÄŃČÜ |
| C | ĀĮ²²åČėĻ”ĻõĖįÖŠ£¬ĪŽĻÖĻó | ĀĮ²±ķĆę±»ĻõĖįŃõ»Æ£¬ŠĪ³ÉÖĀĆܵÄŃõ»ÆĤ |
| D | ±½·ÓČÜŅŗÖŠµĪ¼ÓäåĖ®£¬³öĻÖ°×É«³Įµķ | ±½·ÓŅ×·¢ÉśČ”“ś·“Ó¦ |
| A£® | A | B£® | B | C£® | C | D£® | D |
·ÖĪö A£®¹żĮæĢś·Ū£¬·“Ӧɜ³ÉŃĒĢśĄė×Ó£»
B£®³ĮµķĻņČܽā¶ČøüŠ”µÄ·½Ļņ×Ŗ»Æ£»
C£®³£ĪĀĻĀ£¬ÅØĻõĖįŗĶĀĮ·¢Éś¶Ū»ÆĻÖĻó£»
D£®±½·ÓÓėäå·¢Éś·“Ӧɜ³É2£¬4£¬6-Čżäå±½·Ó£¬ĪŖ°×É«³Įµķ£®
½ā“š ½ā£ŗA£®¹żĮæĢś·Ū£¬·“Ӧɜ³ÉŃĒĢśĄė×Ó£¬¼ÓČėKSCNČÜŅŗ”¢ČÜŅŗ²»ĻŌŗģÉ«£¬¹ŹA“ķĪó£»
B£®³ĮµķĻņČܽā¶ČøüŠ”µÄ·½Ļņ×Ŗ»Æ£¬AgI±ČAgClÄŃČÜ£¬²»·¢Éś×Ŗ»Æ£¬¹ŹB“ķĪó£»
C£®³£ĪĀĻĀ£¬ÅØĻõĖįŗĶĀĮ·¢Éś¶Ū»ÆĻÖĻó£¬Ļ”ĻõĖįŗĶĀĮ·“Ӧɜ³ÉĻõĖįĀĮŗĶNO£¬ÓŠĘųĢåÉś³ÉĒŅĀĮʬ֚½„Čܽā£¬¹ŹC“ķĪó£»
D£®±½·ÓÓėäå·¢Éś·“Ӧɜ³É°×É«³Įµķ2£¬4£¬6-Čżäå±½·Ó£¬ĪŖČ”“ś·“Ó¦£¬¹ŹDÕżČ·£®
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²é½ĻĪŖ×ŪŗĻ£¬Éę¼°Ńõ»Æ»¹Ō·“Ó¦£¬³Įµķ×Ŗ»ÆŅŌ¼°Č”“ś·“Ó¦µČÖŖŹ¶£¬×ŪŗĻæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦”¢ŹµŃéÄÜĮ¦ŗĶĘĄ¼ŪÄÜĮ¦£¬ĪŖøßæ¼³£¼ūĢāŠĶ£¬×¢Ņā°ŃĪÕĪļÖŹµÄŠŌÖŹµÄŅģĶ¬ŅŌ¼°ŹµŃéµÄŃĻĆÜŠŌŗĶæÉŠŠŠŌµÄĘĄ¼Ū£¬ÄŃ¶Č²»“ó£®


 æŖŠÄæģĄÖ¼ŁĘŚ×÷ŅµŹī¼Ł×÷ŅµĪ÷°²³ö°ęÉēĻµĮŠ“š°ø
æŖŠÄæģĄÖ¼ŁĘŚ×÷ŅµŹī¼Ł×÷ŅµĪ÷°²³ö°ęÉēĻµĮŠ“š°ø ĆūĢāѵĮ·ĻµĮŠ“š°ø
ĆūĢāѵĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¶žÕß»„ĪŖĶ¬ĻµĪļ | |
| B£® | ¾ŪŅŅĻ©ŹĒŅŅĻ©µÄĖõ¾Ū²śĪļ | |
| C£® | ¶žÕ߶¼ÄÜŹ¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ« | |
| D£® | µČÖŹĮæµÄŅŅĻ©ŗĶ¾ŪŅŅĻ©·Ö±šĶźČ«Č¼ÉÕĻūŗĵČĪļÖŹµÄĮæµÄŃõĘų£¬Éś³ÉµČĮæµÄĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
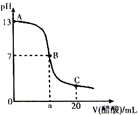 ŌŚ20mL0.100mol•L-1NaOHČÜŅŗÖŠÖšµĪ¼ÓČė0.200mol•L-1“×ĖįČÜŅŗ£¬ĒśĻßČēĶ¼ĖłŹ¾£¬ÓŠ¹ŲĮ£×ÓÅØ¶Č¹ŲĻµ±Č½ĻÕżČ·µÄŹĒ£Ø””””£©
ŌŚ20mL0.100mol•L-1NaOHČÜŅŗÖŠÖšµĪ¼ÓČė0.200mol•L-1“×ĖįČÜŅŗ£¬ĒśĻßČēĶ¼ĖłŹ¾£¬ÓŠ¹ŲĮ£×ÓÅØ¶Č¹ŲĻµ±Č½ĻÕżČ·µÄŹĒ£Ø””””£©| A£® | Aµćµ½BµćµÄ±ä»Æ¹ż³ĢÖŠ£¬Ąė×ÓÅØ¶Č“óŠ”¹ŲĻµ£ŗc£ØNa+£©£¾c£ØCH3COO-£©£¾c£ØOH-£©£¾c£ØH+£© | |
| B£® | ŌŚBµća£¾10£¬ĒŅÓŠc£ØNa+£©=c£ØCH3COO-£©=c£ØOH-£©=c£ØH+£© | |
| C£® | Bµćµ½CµćµÄ±ä»Æ¹ż³ĢÖŠ£¬Ąė×ÓÅØ¶Č“óŠ”¹ŲĻµ£ŗc£ØCH3COO-£©£¾c£ØH+£©£¾c£ØNa+£©£¾c£ØOH-£© | |
| D£® | ŌŚCµć£ŗc£ØCH3COO-£©+c£ØCH3COOH£©=2c£ØNa+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
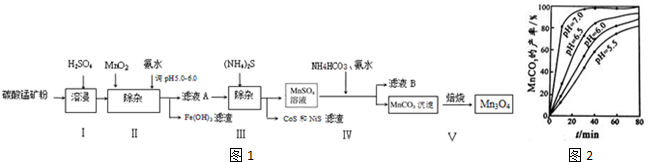
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ĒāĘų ĒāĘų | B£® |  °±Ęų °±Ęų | C£® |  Ė® Ė® | D£® |  ¶žŃõ»ÆĢ¼ ¶žŃõ»ÆĢ¼ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 µÄĻµĶ³ĆüĆūŹĒ2£¬6-¶ž¼×»łŠĮĶé
µÄĻµĶ³ĆüĆūŹĒ2£¬6-¶ž¼×»łŠĮĶé µÄĆū³ĘŹĒ1£¬3-¶ž¼×»ł±½
µÄĆū³ĘŹĒ1£¬3-¶ž¼×»ł±½²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
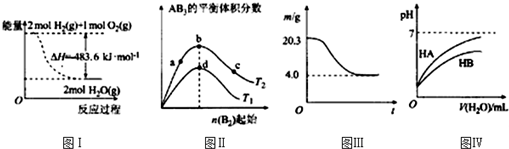
| A£® | Ķ¼¢ń±ķŹ¾H2ÓėO2·¢Éś·“Ó¦¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ£¬ŌņH2µÄČ¼ÉÕČČ”÷H=-241.8 kJ•mol-1 | |
| B£® | Ķ¼¢ņ±ķŹ¾·“Ó¦A2£Øg£©+3B2£Øg£©?2AB3£Øg£©£¬“ļµ½Ę½ŗāŹ±A2µÄ×Ŗ»ÆĀŹ“óŠ”ĪŖ£ŗb£¾a£¾c | |
| C£® | Ķ¼¢ó±ķŹ¾0.1mol MgCl2•6H2OŌŚæÕĘųÖŠ³ä·Ö¼ÓČČŹ±¹ĢĢåÖŹĮæĖꏱ¼äµÄ±ä»Æ | |
| D£® | Ķ¼¢ō±ķŹ¾³£ĪĀĻĀ£¬Ļ”ŹĶHA”¢HBĮ½ÖÖĖįµÄĻ”ČÜŅŗŹ±£¬ČÜŅŗpHĖę¼ÓĖ®ĮæµÄ±ä»Æ£¬ŌņNaAČÜŅŗµÄpH“óÓŚĶ¬ÅضČNaBČÜŅŗµÄpH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com