
水溶液中存在多种平衡,请回答下列问题。
(1)有下列几种溶液:a. NH3·H2O b. CH3COONa c. NH4Cl d. NaHSO4
常温下呈酸性的溶液有 (填序号)。
(2)已知NaHCO3溶液呈碱性,该溶液中除水的电离外还存在着两个平衡,用电离方程式或离子方程式表示: 、
,该溶液中的离子浓度由大到小的顺序是: 。
(3)有浓度均为0.1 mol?L-1的 ①盐酸②硫酸③醋酸三种溶液,请用序号填空:
三种溶液的c(H+)大小顺序为 ;中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次的大小关系为 ;若三种溶液的pH都为2,分别取10mL上述溶液加水稀释至1000mL,此时三种溶液的pH的大小关系为 。
(4)25℃时,AgCl的Ksp=1.8×10-10 ,试写出AgCl溶解平衡的表达式: ,现将足量AgCl固体投入100mL0.1mol/L MgCl2溶液充分搅拌后冷却到25℃时,此时c(Ag+)= mol/L(忽略溶液体积的变化)。
(18分)(每空各2分)(1)c.d (2)HCO3- H++CO32- HCO3-+H2O
H++CO32- HCO3-+H2O H2CO3 +OH— c(Na+)>c(HCO32—)> c(OH—) > c(H+) > c(CO32-)
H2CO3 +OH— c(Na+)>c(HCO32—)> c(OH—) > c(H+) > c(CO32-)
(3)②>①>③ ①=③>② ①=②>③
(4)AgCl(S) Ag+(aq)+Cl-(aq) 9×10-10
Ag+(aq)+Cl-(aq) 9×10-10
解析试题分析:(1)氨水是弱碱,溶液显碱性。醋酸钠溶于水,CH3COO-发生水解,溶液显碱性。氯化铵溶于水,NH4+发生水解,溶液显酸性。硫酸氢钠盐,溶于水,完全电离出氢离子,溶液显酸性,答案选cd。
(2)碳酸氢钠是弱酸的酸式盐,既有HCO3-的水解平衡,也有HCO3-的电离平衡,有关的离子方程式是HCO3- H++CO32-、HCO3-+H2O
H++CO32-、HCO3-+H2O H2CO3 +OH—。由于水解程度,大于电离程度,所以溶液显碱性,有关离子浓度的大小关系是c(Na+)>c(HCO32—)> c(OH—) > c(H+) > c(CO32-)。
H2CO3 +OH—。由于水解程度,大于电离程度,所以溶液显碱性,有关离子浓度的大小关系是c(Na+)>c(HCO32—)> c(OH—) > c(H+) > c(CO32-)。
(3)盐酸是一元缺少,硫酸是二元强酸,醋酸是一元弱酸,所以在物质的量浓度相等的条件下,三种溶液的c(H+)大小顺序为②>①>③;中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次的大小关系为①=③>②;在稀释过程中,醋酸内继续电离出氢离子,所以稀释后三种溶液的pH的大小关系为①=②>③。
(4)AgCl溶解平衡的表达式为AgCl(S) Ag+(aq)+Cl-(aq)。溶液中氯离子的浓度是0.2mol/L,则根据氯化银的溶度积常数可知,溶液中c(Ag+)=
Ag+(aq)+Cl-(aq)。溶液中氯离子的浓度是0.2mol/L,则根据氯化银的溶度积常数可知,溶液中c(Ag+)=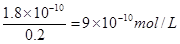
考点:考查溶液酸碱性的判断、碳酸氢钠的水解和电离、弱电解质的电离平衡以及溶度积常数的有关计算和应用
点评:该题是中等难度的试题,试题注重基础性知识的检查和巩固。该题考查的知识点比较分散,主要是围绕弱电解质的电离平衡和溶解平衡展开的,有利于培养学生的逻辑思维能力和发散思维能力,提高学生分析问题、归纳、总结问题的能力。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
| 资料:①H2S可溶于水(约1:2),其水溶液为二元弱酸. ②H2S可与许多金属离子反应生成沉淀. ③H2S在空气中燃烧,火焰呈淡蓝色. |
| 实验操作 | 实验现象 | |
| 实验1 | 将等浓度的Na2S和Na2SO3溶液按体积比2:1混合 | 无明显现象 |
| 实验2 | 将H2S通入Na2SO3溶液中 | 未见明显沉淀,再加入少量稀硫酸,立即产生大量浅黄色沉淀 |
| 实验3 | 将SO2通入Na2S溶液中 | 有浅黄色沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 通过实验测定反应速率的方法有多种,为证明化学反应速率与反应的浓度有关.有同学设计如下实验:
通过实验测定反应速率的方法有多种,为证明化学反应速率与反应的浓度有关.有同学设计如下实验:| 序号 | Na2S2O3溶液 | 稀H2SO4 | 出现混浊时间 | ||
| 浓度 | 用量 | 浓度 | 用量 | ||
| (1) | 0.1mol?L-1 | 10mL | 0.1mol?L-1 | 10mL | t1 |
| (2) | 0.1mol?L-1 | 10mL+5mL 水 | 0.1mol?L-1 | 10mL | t2 |
| (3) | 0.1mol?L-1 | 10mL | 0.1mol?L-1 | 5mL+5mL水 | t3 |
| (4) | 0.1mol?L-1 | 5mL | 0.1mol?L-1 | 5mL | t4 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省凉山州高三第二次诊断性测试理综化学试卷(解析版) 题型:实验题
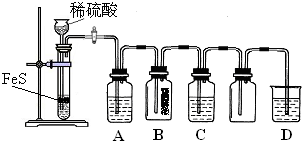
2012年10月8日发布的修订版《机动车驾驶证申领和使用规定》,以其对违章驾驶员的严厉惩罚被人们称为“史上最严交规”,其中饮酒后驾驶机动车的一次记12分。利用如下测试管可检测司机是否酒后驾车,化学原理如下:

金属铬在化合物中主要有+3价和+6价两种价态。+6价铬化合物K2CrO4和K2Cr2O7在水溶液中分别呈黄色和橙色,它们在溶液中存在如下平衡关系:2CrO42-+2H+ Cr2O72-+H2O在酸性条件下+6价铬化合物具有强氧化性,可以将C2H5OH氧化为CH3COOH,本身被还原为Cr3+,Cr3+在水溶液中呈灰绿色。
Cr2O72-+H2O在酸性条件下+6价铬化合物具有强氧化性,可以将C2H5OH氧化为CH3COOH,本身被还原为Cr3+,Cr3+在水溶液中呈灰绿色。
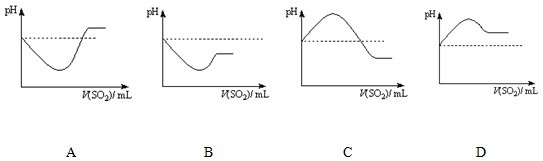
(1)根据上述条件可知,在强酸性条件下+6价铬主要以 (填“CrO2-4”或“Cr2O2-7”)形式存在。如果司机酒后驾车,则测试管中的现象是 且超过法定警界线,反应的离子方程式为 。
(2)研究发现+6价铬的毒性为+3价铬的毒性的100~200倍,有多种方法可以将废水中的+6价铬转化为+3价铬以降低毒性。其中两种方法如下:
方法一:电化学方法。将含Cr2O2-7的酸性废水加适量NaCl搅拌均匀并以Fe作电极进行电解。在阳极产生的Fe2+将Cr2O2-7还原为Cr3+,在电解过程中溶液的pH不断上升,最终Cr3+和Fe3+以Cr(OH)3和Fe(OH)3沉淀的形式析出。
①请分析溶液pH不断上升的原因: 。
②已知Fe3+和Cr3+变为Fe(OH)3和Cr(OH)3沉淀的pH如下表:

当溶液的pH范围为____时,溶液中Fe3+已沉淀完全而Cr3+还没有开始沉淀。
③当电路中通过3mol电子时,理论可还原Cr2O2-7的物质的量为 mol。
方法二:还原沉淀法。将l0ml某含铬(Cr2O2-7)废水用硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀,该沉淀经干燥后为nmolFeO·FeyCrxO3。
④不考虑处理过程中的实际损耗,下列叙述错误的是
A.反应中发生转移的电子个数为3nx
B.该废水中c(Cr2O2-7)为50nx mol/L
C.消耗硫酸亚铁铵的物质的量为n(l+y)mol
D.在FeO·FeyCrxO3中,x+y=2
查看答案和解析>>
科目:高中化学 来源:2014届黑龙江哈尔滨第十二中学高二上学期期末考试化学试卷(解析版) 题型:填空题
水溶液中存在多种平衡,请回答下列问题。
(1)有下列几种溶液:a. NH3·H2O b. CH3COONa c. NH4Cl d. NaHSO4
常温下呈酸性的溶液有 (填序号)。
(2)已知NaHCO3溶液呈碱性,该溶液中除水的电离外还存在着两个平衡,用电离方程式或离子方程式表示: 、
,该溶液中的离子浓度由大到小的顺序是: 。
(3)有浓度均为0.1 mol?L-1的 ①盐酸②硫酸③醋酸三种溶液,请用序号填空:
三种溶液的c(H+)大小顺序为 ;中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次的大小关系为 ;若三种溶液的pH都为2,分别取10mL上述溶液加水稀释至1000mL,此时三种溶液的pH的大小关系为 。
(4)25℃时,AgCl的Ksp=1.8×10-10 ,试写出AgCl溶解平衡的表达式: ,现将足量AgCl固体投入100mL0.1mol/L MgCl2溶液充分搅拌后冷却到25℃时,此时c(Ag+)= mol/L(忽略溶液体积的变化)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com