
某同学用工业硫酸铜(含硫酸亚铁等杂质)制备纯净的CuSO4·5H2O。工艺流程如下
(部分操作和条件略):
I.取工业硫酸铜固体,用稀硫酸溶解,过滤。
II.向滤液中滴加H2O2溶液,稍加热。
III.向II的溶液中加入CuO粉末至pH=4。
IV.加热煮沸,过滤,滤液用稀硫酸酸化至pH=1。
V.蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得晶体。
已知部分阳离子生成氢氧化物的pH、Ksp(25℃)如下表:
物质 | Fe(OH)3 | Fe (OH)2 | Cu(OH)2 |
开始沉淀时pH | 2.7 | 7.6 | 4.7 |
完全沉淀时pH | 3.7 | 9.6 | 6.7 |
Ksp | 4.0×10–38 | 8.0×10–16 | 2.2×10–20 |
(1)II中发生反应的离子方程式是 。
(2)II中将Fe2+氧化为Fe3+的目的是 。
(3)用K3[Fe(CN)6](铁氰化钾)验证II中Fe2+是否转化完全的现象是 。
(4)III中发生反应的离子方程式是 。
通过计算说明在此条件下的溶液中Fe3+是否沉淀完全________________________(提示:当溶液中某离子浓度小于1.0×10–5 mol/L时可认为该离子沉淀完全)。
(5)应用化学平衡移动原理解释IV中“滤液用稀硫酸酸化”的原因 。
(1)2Fe2+ +H2O2+2H+=2Fe3++2H2O (2分) (2)在调节pH=4时,只将Fe3+转化为沉淀除去,而不会使Cu2+转化为沉淀。(表述合理即可得分) (2分)
(3)若有蓝色沉淀生成,说明Fe2+没有完全转化;若没有蓝色沉淀生成,说明Fe2+已经完全转化。(只答出其中一种情况,表述正确得满分。) (1分)
(4)Fe3++3H2O Fe(OH)3+3H+ CuO+2H+=Cu2++ H2O (或只书写第二个反应也可得分)
Fe(OH)3+3H+ CuO+2H+=Cu2++ H2O (或只书写第二个反应也可得分)
或2Fe3++3CuO+3H2O=2Fe(OH)3+3Cu2+ (2分)
c(Fe3+)=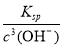 =4.0×10–8 mol·L–1<1.0×10–5 mol·L–1,故Fe3+沉淀完全 (2分)
=4.0×10–8 mol·L–1<1.0×10–5 mol·L–1,故Fe3+沉淀完全 (2分)
(5)用稀硫酸酸化至pH=1,可以抑制Cu2+在加热过程中水解,以获得纯净的硫酸铜晶体。(表述合理即可得分) (1分)
【解析】
试题分析:(1)由于溶液中含有亚铁离子,需要将其氧化为铁离子除去。双氧水具有氧化性,因此向滤液中滴加H2O2溶液,稍加热的目的是除去亚铁离子,反应的离子方程式为2Fe2+ +H2O2+2H+=2Fe3++2H2O。
(2)由于亚铁离子沉淀时的pH值大于铜离子沉淀时的pH值,而铁离子完全沉淀时的pH值是3.7,所以II中将Fe2+氧化为Fe3+的目的是在调节pH=4时,只将Fe3+转化为沉淀除去,而不会使Cu2+转化为沉淀。
(3)由于铁氰化钾与亚铁离子结合产生蓝色沉淀,据此可以检验亚铁离子。即若有蓝色沉淀生成,说明Fe2+没有完全转化;若没有蓝色沉淀生成,说明Fe2+已经完全转化。
(4)氧化铜能消耗氢离子,降低溶液的酸性,从而产生氢氧化铁沉淀,因此反应的离子方程式为Fe3++3H2O Fe(OH)3+3H+ CuO+2H+=Cu2++ H2O;氢氧化铁的溶度积常数是4.0×10–38,则当溶液中OH-等于10-10mol/L时,则此时溶液中c(Fe3+)=
Fe(OH)3+3H+ CuO+2H+=Cu2++ H2O;氢氧化铁的溶度积常数是4.0×10–38,则当溶液中OH-等于10-10mol/L时,则此时溶液中c(Fe3+)=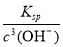 =4.0×10-8 mol·L-1<1×10-5 mol·L-1,故Fe3+沉淀完全。
=4.0×10-8 mol·L-1<1×10-5 mol·L-1,故Fe3+沉淀完全。
(5)由于铜离子水解,溶液显酸性,所以用稀硫酸酸化至pH=1,可以抑制Cu2+在加热过程中水解,以获得纯净的硫酸铜晶体。
考点:考查硫酸铜晶体制备、氧化还原反应、亚铁离子检验、盐类水解以及溶度积常数的有关计算


科目:高中化学 来源:2015届湖北省荆门市高二上学期期末考试化学试卷(解析版) 题型:实验题
某实验小组设计用50 mL 1.0 mol/L盐酸跟50 mL 1.1 mol/L 氢氧化钠溶液在如图装置中进行中和反应。在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过。通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:
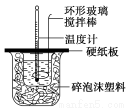
(1)本实验中用稍过量的NaOH的原因教材中说是为保证盐酸完全被中和。试问:盐酸在反应中若因为有放热现象,而造成少量盐酸在反应中挥发,则测得的中和热 (填“偏大”、“偏小”或“不变”)。
(2)在中和热测定实验中存在用水洗涤温度计上的盐酸的步骤,若无此操作步骤,则测得的中和热会 (填“偏大”、“偏小”或“不变”)。
(3)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会 (填“偏大”、“偏小”或“不变”),其原因是 。
(4)该实验小组做了三次实验,每次取溶液各50 mL,并记录下原始数据(见下表)。
实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差(t2-t1)/℃ | ||
盐酸 | NaOH溶液 | 平均值 | |||
1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
已知盐酸、NaOH溶液密度近似为1.00g/cm3,中和后混合液的比热容c=4.18×10-3kJ/(g·℃),则该反应的中和热为ΔH= 。根据计算结果,写出该中和反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015届湖北省荆州市部分县市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列事实解释准确的是
A.糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。脱氧过程中铁作原电池正极,电极反应为:Fe-2 e-=Fe2+
B.酸性氢氧燃料电池的正极电极反应为:2H2O+O2+4e-=4OH-
C.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,该反应的△S>0,说明反应△H>0
D.铅蓄电池的正极反应为:PbO2+4H++2 e-=Pb2++2H2O
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高二上学期期末考试化学试卷(解析版) 题型:选择题
建筑用的钢材在出厂前都要经过烤蓝处理,使其表面生成一层四氧化三铁,其目的是
A.增加钢材的硬度 B.增强钢材的抗腐蚀能力
C.使钢材美观 D.增加钢材的韧性
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高二上学期期末考试化学试卷(解析版) 题型:选择题
将铁粉和硫粉混合无明显现象,加热,待反应一发生就立刻停止加热,反应可以持续进行,直至完全生成新物质硫化亚铁。该现象说明了
A.该反应是分解反应
B.该反应是放热反应
C.该反应生成物的化学式为 Fe2S3
D.生成物硫化亚铁的总能量高于反应物铁粉和硫粉的总能量
查看答案和解析>>
科目:高中化学 来源:2015届湖北省三校高二上学期期末联考化学试卷(解析版) 题型:选择题
下列实验操作导致所读出数值比真实值小的是(假设其他操作均正确)
A.对滴定管仰视读数:18.80 mL
B.用蒸馏水润湿pH试纸测定某浓度的硫酸溶液的pH=5
C.用量筒量取饱和食盐水时,俯视读数:8.8 mL
D.中和热测定时,用铜棒代替环形玻璃搅拌棒搅拌,测定反应的最高温度:38.8℃
查看答案和解析>>
科目:高中化学 来源:2015届湖北省三校高二上学期期末联考化学试卷(解析版) 题型:选择题
组成为C10H14的芳香烃,其苯环上有两个取代基时的同分异构体数目为
A.6种 B.9种 C.12种 D.15种
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
烃A最多可以与两倍于其物质的量的H2加成,当烃A与足量HCl加成后产物为B,B与四倍于其物质的量的Cl2反应才能得到完全卤代的产物,A是
A.1,3-丁二烯 B.乙炔 C.丁炔 D.乙烯
查看答案和解析>>
科目:高中化学 来源:2015届浙江省慈溪市高二上学期期末测试化学试卷(解析版) 题型:选择题
钓鱼岛群岛的东海海域及部分太平洋海域探明为海底热水矿床.海底热水矿床是沉积着由岩浆热气从地底喷出金、铜、锌、稀有金属等区域.下列说法正确的是
A.金不溶于任何溶液
B.铜、锌在空气中被氧化后的最后产物均为对应的氧化物
C.铜锌合金的熔点低于铜或锌的熔点
D.稀有金属原子 质子数和中子数之差为28
质子数和中子数之差为28
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com