
| ���� | �ݻ�/L | �¶�/�� | ��ʼ��/mol | ƽ����/mol | |
| C��s�� | H2O��g�� | H2��g�� | |||
| �� | 2 | T1 | 2 | 4 | 3.2 |
| �� | 1 | T2 | 1 | 2 | 1.2 |
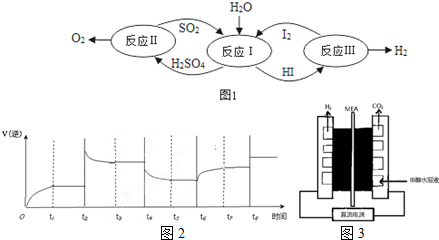
���� ��1���ٸ���ͼ֪��SO2��I2��H2O�Ƿ�Ӧ�HI��H2SO4����������ݷ�Ӧ�����������д����ʽ��H2SO4��c��H+����c��SO42-��=2��1����HI����������ӣ�
��a.2H2SO4��l���T2SO2��g��+O2��g��+2H2O��g����H=+550kJ•mol-1
b��H2SO4��l���TSO3��g��+H2O��g����H=+177kJ•mol-1
������ʽa-2b��2SO3��g��?2SO2��g��+O2��g���ʱ������Ӧ�ĸı䣻
��2������������ʽ����ƽ��ʱ����ֵ����ʵ������ٸ���ƽ�ⳣ��k���㣻�ӱ������ݿ�֪�������������з�Ӧ��Ũ����ͬ���Ҵﵽƽ��ʱH2��g����ƽ�����ȼ�һ��С����T2��T1ƽ�������ƶ�������֪�÷�Ӧ����Ϊ���ȷ�Ӧ����T2��T1�ǽ����¶ȣ�˵��T2�¶ȵͣ�
���淴Ӧ���У����ʵ�Ũ�Ƚ��ͣ���Ӧ���ʽ϶̣���ǰ1.5minˮ��Ũ�ȱ仯�����ں�1.5minˮ��Ũ�ȱ仯�����ݴ˽��
�۸÷�Ӧ��һ����Ӧǰ����������������������Ӧ�����ȵĻ�ѧ��Ӧ��t2ʱ�淴Ӧ����������ƽ��ʱ��Ӧ���ʴ���t2ʱ��Ӧ���ʣ�ƽ�����淴Ӧ�����ƶ���t8ʱ��Ӧ��������ƽ�ⲻ�ƶ���������������Ի�ѧ��Ӧ���ʵ�Ӱ�����������
��3���ٸ���ͼ3��֪����ӦΪ�״�ʧ���ӵõ�CO2��
�ںϽ������õ�����һ�ֽ������⻯����������������Ϊ0.077��һ�ֽ������ʣ��ݴ��Ƴ�MgH2��Al���ɴ�д����Ӧ����ʽ��
��� �⣺��1���ٸ���ͼ֪��SO2��I2��H2O�Ƿ�Ӧ�HI��H2SO4����������ݷ�Ӧ�����������д����ʽΪSO2+I2+2H2O=2HI+H2SO4�����ӷ���ʽΪ��SO2+2H2O+I2=SO42-+2I-+4H+��H2SO4����c��H+����c��SO42-��=2.06��1�����ֵ����2��ԭ����������к�������HI����HI����������ӣ�
�ʴ�Ϊ��SO2+2H2O+I2=SO42-+2I-+4H+��������к�������HI����HI����������ӣ�
��a.2H2SO4��l���T2SO2��g��+O2��g��+2H2O��g����H=+550kJ•mol-1
b��H2SO4��l���TSO3��g��+H2O��g����H=+177kJ•mol-1
������ʽa-2b��2SO3��g��?2SO2��g��+O2��g����H=��+550kJ•mol-1��-2��+177kJ•mol-1��=+196 kJ•mol-1��
�ʴ�Ϊ��2SO3��g��?2SO2��g��+O2��g����H=+196 kJ•mol-1��
��2�����ɱ������ݿ�֪��ƽ��ʱ���������ʵ���Ϊ3.2mol����
C��s��+2H20��g��?C02��g��+2H2��g��
��ʼ��mol����2 4 0 0
ת����mol����1.6 3.2 1.6 3.2
ƽ�⣨mol����0.4 0.8 1.6 3.2
ƽ�ⳣ��k=$\frac{c��C{O}_{2}��{c}^{2}��{H}_{2}��}{{c}^{2}��{H}_{2}O��}$=$\frac{\frac{1.6}{2}����\frac{3.2}{2}��^{2}}{��\frac{0.8}{2}��^{2}}$=12.8��
�ӱ������ݿ�֪�������������з�Ӧ��Ũ����ͬ���Ҵﵽƽ��ʱH2��g����ƽ�����ȼ�һ��С����T2��T1ƽ�������ƶ�������֪�÷�Ӧ����Ϊ���ȷ�Ӧ����T2��T1�ǽ����¶ȣ�˵��T2�¶ȵͣ�
�ʴ�Ϊ��12.8������
��3min��ˮ������Ũ�ȱ仯��=������Ũ�ȱ仯����һ��=$\frac{1.2mol}{1L}$��$\frac{1}{2}$=0.6mol/L���淴Ӧ���У����ʵ�Ũ�Ƚ��ͣ���Ӧ���ʽ϶̣���ǰ1.5minˮ��Ũ�ȱ仯�����ں�1.5minˮ��Ũ�ȱ仯�����ʷ�Ӧ���е�1.5minʱ��H2O��g�������ʵ���Ũ��С��2mol/L-0.6mol/L=1.4mol/L��
�ʴ�Ϊ��B��
��t1��t6ƽ�ⶼ�����ƶ�����t6ʱƽ�������ƶ�������Ϊ���ӷ�Ӧ���Ũ�ȣ���C�ǹ��壬����������ˮ�������������Ա�����ת���ʽ��ͣ�t8ʱ��Ӧ��������ƽ�ⲻ�ƶ�����ƽ��ת�������t7-t8 ����t7��t8������t4ʱ�����ʶ���ԭ������С��ƽ�����������ǽ����¶ȣ�
�ʴ�Ϊ��t7-t8�������¶ȣ�
��3���ٸ���ͼ3��֪����ӦΪ�״�ʧ���ӵõ�CO2����������ӦʽΪCH3OH+H2O-6e-=CO2��+6H+��
�ʴ�Ϊ��CH3OH+H2O-6e-=CO2��+6H+��
�ںϽ������õ�����һ�ֽ������⻯����������������Ϊ0.077��һ�ֽ������ʣ��ݴ��Ƴ�MgH2��Al���ɴ�д����Ӧ����ʽΪMg17Al12+17H2=17MgH2+12Al��
�ʴ�Ϊ��Mg17Al12+17H2=17MgH2+12Al��
���� ���⿼�����Ȼ�ѧ����ʽ��˹���ɵļ���Ӧ�ã���ѧƽ�ⳣ����Ӱ�������жϣ�����ƽ�⣬����ƴ������Ŀ����ѧ���������нϸߵ�Ҫ�����ջ����ǹؼ����Ѷ��еȣ�


 Сѧ��ĩ���Ծ�ϵ�д�
Сѧ��ĩ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
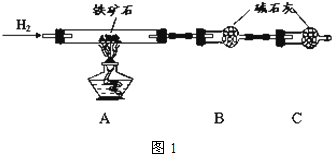 ����ʯ�ǹ�ҵ��������Ҫԭ��֮һ������Ҫ�ɷ�Ϊ����������������в�����Ԫ�غ���Ԫ�أ������ʲ���H2SO4��Ӧ����ij�о���ѧϰС���ij����ʯ������������Ļ�ѧʽ����̽����
����ʯ�ǹ�ҵ��������Ҫԭ��֮һ������Ҫ�ɷ�Ϊ����������������в�����Ԫ�غ���Ԫ�أ������ʲ���H2SO4��Ӧ����ij�о���ѧϰС���ij����ʯ������������Ļ�ѧʽ����̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ԫ�ر�� Ԫ������ | �� | �� | �� | �� | �� |
| ԭ�Ӱ뾶/nm | 0.037 | 0.110 | 0.077 | 0.099 | 0.186 |
| ���ֻ��ϼ� | +1 | -3+5 | -4+4 | -1 | +1 |
| A�� | �������ڱ��зǽ�������ǿ��Ԫ�� | |
| B�� | �������ڱ���ԭ�Ӱ뾶��С��Ԫ�� | |
| C�� | �ڢܢ���λ��ͬһ������ | |
| D�� | �٢���Ԫ����ɵ�������������ۢ���Ԫ����ɵĻ�������ӿռ乹����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ij��ѧ��ȤС��������ͼװ���Ʊ��������������۲�����ɫ���ṩ��ѧҩƷ����м��ϡ���ᡢ����������Һ��
ij��ѧ��ȤС��������ͼװ���Ʊ��������������۲�����ɫ���ṩ��ѧҩƷ����м��ϡ���ᡢ����������Һ��| ʵ����� | ��һ�� | �ڶ��� | ������ |
| ���ĸ��������Һ���/mL | 25.52 | 25.02 | 24.98 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ͼ��ʾ��ͭ-пԭ����У�
��ͼ��ʾ��ͭ-пԭ����У��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ŵ�ʱ��LiMn2O4����������Ӧ | |
| B�� | �ŵ�ʱ��������ӦΪ��Li++LiMn2O4+e-�TLi2Mn2O4 | |
| C�� | ���ʱ��LiMn2O4����������Ӧ | |
| D�� | ���ʱ��������ӦΪ��Li++e-�TLi |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ɫ�������������ܶȶ���ˮС | |
| B�� | �����ڿ�����ȼ�����ɵĶ��ǹ������� | |
| C�� | ���ʵ��۷е�����ԭ�����������Ӷ����� | |
| D�� | �����������ˮ���ҷ�Ӧ���ɼ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com