
| A. | 钠的还原性很强,可以用来冶炼金属钛、锆、铌等 | |
| B. | 钠的化学性质非常活泼,钠元素只能以化合态存在于自然界 | |
| C. | 钠极易和水反应而被还原 | |
| D. | 钠、氧化钠、氢氧化钠的焰色反应均显黄色 |
分析 A.钠比较活泼,可用来置换较难冶炼的较不活泼金属;
B.钠的化学性质非常活泼,易失去最外层电子而被氧化生成化合物;
C.钠和水反应失电子体现还原性;
D.焰色反应是元素的性质,无论元素处于什么样的状态都有同样的焰色;
解答 解:A.钠比钛、锆、铌等金属活泼,并且钛、锆、铌等金属较难冶炼,可用钠置换,故A正确;
B.钠的化学性质非常活泼,易失去最外层电子而被氧化生成化合物,在自然界中只能以化合态存在,故B正确,
C.钠极易和水反应失电子而被氧化,故C错误;
D.焰色反应是元素的性质,无论元素处于什么样的状态都有同样的焰色,所以钠、氧化钠、氢氧化钠的焰色反应均显黄色,故D正确.
故选C.
点评 本题考查钠的性质,题目难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
| X | ||
| Y | ||
| Z |
| A. | X是活泼的非金属元素,其最高价氧化物的水化物是一种强酸 | |
| B. | Y是最活泼的非金属元素,不存在最高价氧化物的水化物 | |
| C. | Z是较活泼的非金属元素,其最高价氧化物的水化物是一种强酸 | |
| D. | X、Y、Z的单质中Z的熔点最高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | X | |
| Y | Z |
| A. | X、Y、Z中最简单氢化物稳定性最弱的是Y | |
| B. | Z元素氧化物对应水化物的酸性一定强于Y | |
| C. | X元素形成的单核阴离子还原性强于Y | |
| D. | Z元素单质在化学反应中只表现氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
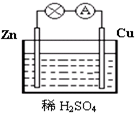 图为原电池的示意图.请回答:
图为原电池的示意图.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
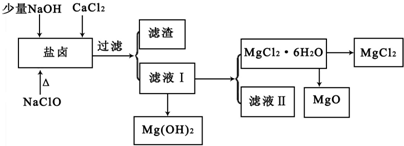
| pH | <8.0 | 8.0~9.6 | >9.6 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2的电子式为 Na${\;}_{•}^{•}$$\stackrel{••}{O}$${\;}_{•}^{•}$${\;}_{•}^{•}$$\stackrel{••}{O}$${\;}_{•}^{•}$Na | |
| B. | NH4Br的电子式: +Br- +Br- | |
| C. | 氢氧根离子的电子式:[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$H]- | |
| D. | HClO的电子式:H${\;}_{•}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ⑤⑥ | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com