
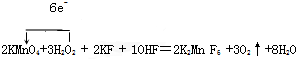 ,故答案为:
,故答案为: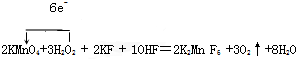 ;
;

 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源: 题型:
| A、油脂在碱性条件下水解可制得肥皂 |
| B、海轮外壳上镶入锌块,可减缓船体的腐蚀 |
| C、人体中缺碘元素会得贫血病 |
| D、研制推广甲醇燃料汽车,有利于“减排目标”的实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验次数 | B与混合气体的体积比 | 反应后气体密度(已换算为标准状况;g/L) |
| 第一次 | 1.0 | 1.35 |
| 第二次 | 1.2 | 1.25 |
| 第三次 | 2.0 | 1.04 |
| 第四次 | 2.2 | -- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 PPA是抗感冒药中禁止添加的物质.已知PPA由四种元素构成,且这四种元素均位于元素周期表的前两周期,其比例模型如图所示.下列有关PPA的说法中正确的是( )
PPA是抗感冒药中禁止添加的物质.已知PPA由四种元素构成,且这四种元素均位于元素周期表的前两周期,其比例模型如图所示.下列有关PPA的说法中正确的是( )| A、PPA的分子式为C9H12NO |
| B、PPA既能与盐酸反应,又能与氢氧化钠溶液反应 |
| C、PPA能发生酯化反应 |
| D、PPA分子中所有碳原子一定在同一平面上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com